题目内容
15.有一混合物水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Fe3+、CO32-、SO42-,现各取100ml溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生②向第二份加入足量NaOH溶液后加热,收集到气体0.896L(标准状况)③向第三份加入足量BaCl2溶液,得到沉淀6.27克,沉淀经足量盐酸洗涤后,剩余2.33克.试回答下列问题:
(1)肯定存在的离子有K+、NH4+、CO32-、SO42-,肯定不存在的离子有Fe3+、Mg2+,
(2)可能存在的离子是Cl-,
(3)试分别确定肯定存在的阳离子在原溶液中各自的物质的量浓度.
分析 由①实验可知,向第一份溶液中加入AgNO3溶液,有白色沉淀产生,白色沉淀为AgCl或碳酸银、硫酸银;
由②可知,向第二份溶液中加入足量NaOH 溶液后加热,收集到0.896L(标准状况)气体,气体为氨气,其物质的量为$\frac{0.896L}{22.4L/mol}$=0.04mol,原溶液中一定含NH4+;
由③可知,向第三份溶液中加入足量BaCl2溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后剩余2.33g,则含SO42-的物质的量为$\frac{2.33g}{233g/mol}$=0.01mol,含CO32-的物质的量为$\frac{6.27g-2.33g}{197g/mol}$=0.02mol,结合离子共存、电荷守恒解答.
解答 解:由①实验可知,向第一份溶液中加入AgNO3溶液,有白色沉淀产生,白色沉淀为AgCl或碳酸银、硫酸银;
由②可知,向第二份溶液中加入足量NaOH 溶液后加热,收集到0.896L(标准状况)气体,气体为氨气,其物质的量为$\frac{0.896L}{22.4L/mol}$=0.04mol,原溶液中一定含NH4+;
由③可知,向第三份溶液中加入足量BaCl2溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后剩余2.33g,则含SO42-的物质的量为$\frac{2.33g}{233g/mol}$=0.01mol,含CO32-的物质的量为$\frac{6.27g-2.33g}{197g/mol}$=0.02mol,由离子共存可知,一定不存在Fe3+、Mg2+,由电荷守恒可知,0.01mol×2+0.02mol×2>0.04mol,可知一定含阳离子K+,不能确定是否含Cl-,
(1)由上述分析可知,一定存在K+、NH4+、CO32-、SO42-,一定不存在Fe3+、Mg2+,
故答案为:K+、NH4+、CO32-、SO42;Fe3+、Mg2+;
(2)由上述分析可知,可能存在Cl-,
故答案为:Cl-;
(3)依据计算可知铵根离子浓度c(NH4+)=$\frac{0.04mol}{0.1L}$=0.4mol/L,根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol,c(-)=2c(CO32-)+2c(SO42-)=0.06mol,总正电荷小于负电荷,则原溶液中一定含有K+,至少为0.02mol,C(K+)≥0.2mol/L,
答:肯定存在的阳离子在原溶液中各自的物质的量浓度C(K+)≥0.2mol/L、C(NH4+)=0.4mol/L;
点评 本题考查物质的检验及推断,为高频考点,把握现象与反应、离子推断的关系为解答的关键,实验③中白色沉淀为解答的突破口,侧重分析与计算、推断能力的考查,注意电荷守恒的应用,题目难度中等.

 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 ,其中苯环上的氢原子如果被氯原子取代,所得物质的毒性是KCN的100倍.当两个氯原子取代苯环上的氢时,所得同分异构体的数目是( )
,其中苯环上的氢原子如果被氯原子取代,所得物质的毒性是KCN的100倍.当两个氯原子取代苯环上的氢时,所得同分异构体的数目是( )| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
| A. | 在多电子的原子里,能量低的电子通常在离核近的区域内运动 | |
| B. | 氯化氢溶于水后能电离出H+、Cl-,故HCl 属于离子化合物 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 固体烧碱既含有离子键,也含有非极性共价键 |
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 20℃时,1 L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA | |
| C. | 1 mol甲基含10 NA个电子 | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| A. | 从海水中提炼出的氘(含 HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题, 成为一条新的科学思路.HDO与 H2O化学性质相同 | |
| B. | 从海水中提取镁可以采用下列方法:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液→MgCl2•6H2O$→_{△}^{HCl}$MgCl2(熔融)$\stackrel{电解}{→}$Mg | |
| C. | 从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,已知该化合物中碘元素呈+3和+5两种价态,则这种化合物的化学式是 I4O9 | |
| D. | 除去粗盐中的 SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
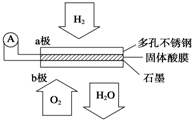 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,完成下列问题:
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,完成下列问题: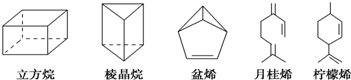
 某有机物的结构如图所示,它不可能具有的性质是( )
某有机物的结构如图所示,它不可能具有的性质是( )