题目内容
下列说法正确的是( )
| A、标准状况下,28 g CO与N2的混合气体的体积约为22.4 L |
| B、0.5 mol H2所占的体积是11.2 L |
| C、标准状况下,1 mol H2O的体积为22.4 L |
| D、标准状况下,6.02×1023个分子所占的体积约是22.4 L |
考点:气体摩尔体积
专题:
分析:A.N2和CO摩尔质量相同为28g/mol,依据n=
计算物质的量得到气体在标准状况下的体积;
B.依据气体摩尔体积的条件应用分析判断;
C.标准状况水不是气体;
D.依据气体摩尔体积的条件应用分析判断.
| m |
| M |
B.依据气体摩尔体积的条件应用分析判断;
C.标准状况水不是气体;
D.依据气体摩尔体积的条件应用分析判断.
解答:
解:A.在标准状况下,28 g的N2和CO的混合气体,N2和CO摩尔质量相同为28g/mol,物质的量为1mol,其体积约为22.4 L,故A正确;
B.标准状况下,0.5mol H2所占的体积一定是11.2L,温度压强不知,0.5mol氢气体积不是11.2L,故B错误;
C.在标准状况下,水不是气体,1mol水的体积不是22.4 L,故C错误;
D.标准状况下,分子不一定是气体,1mol的体积不一定是22.4 L,故D错误;
故选A.
B.标准状况下,0.5mol H2所占的体积一定是11.2L,温度压强不知,0.5mol氢气体积不是11.2L,故B错误;
C.在标准状况下,水不是气体,1mol水的体积不是22.4 L,故C错误;
D.标准状况下,分子不一定是气体,1mol的体积不一定是22.4 L,故D错误;
故选A.
点评:本题考查了气体摩尔体积的条件分析应用,难度不大.掌握概念的实质和应用条件是解题关键.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列分子中,所有原子都满足最外层为8电子结构的是( )
| A、BF3 |
| B、PCl5 |
| C、HCl |
| D、CF2Cl2 |
下列溶液中的c(Cl-)与300ml 1mol/L的AlCl3溶液中的c(Cl-)相同的是( )
| A、150 mL 1mol/L NaCl溶液 |
| B、150 mL 2mol/L CaCl2溶液 |
| C、150 mL 3mol/L KCl溶液 |
| D、300 mL 1mol/L MgCl2溶液 |
下列化学用语表示正确的是( )
A、甲基的电子式: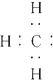 |
B、氮原子的电子排布图: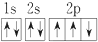 |
| C、氯离子的最外层电子排布:3s23p6 |
D、硫原子的结构示意图: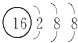 |
设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
| A、1 mol苯分子中含有C=C双键数为3NA |
| B、1mol羟基(-OH)所含的电子总数为10NA |
| C、标准状况下,2.24L甲醇中含有C-H键的数目为0.3NA |
| D、5.6g乙烯和丙烯的混合气体中所含碳原子数为0.4NA |
下列表示对应化学反应的离子方程式正确的是( )
| A、铜溶于FeCl3溶液:Cu+Fe3+=Cu2++Fe2+ |
| B、Na[Al(OH)4]溶液中通入过量CO2:[Al(OH)4]-+CO2=Al(OH)3↓+CO32- |
| C、氯化铝溶液中加过量氨水:Al3++3OH-═Al(OH)3↓ |
| D、次氯酸钠溶液中滴入浓盐酸产生氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
下列有关叙述正确的是( )
| A、元素原子最外层电子数的多少是判断金属性和非金属性强弱的依据 |
| B、OH-与H3O+组成元素相同,所含质子数相同 |
C、结构示意图为 和 和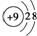 两种粒子为同一种元素 两种粒子为同一种元素 |
| D、H、D、T具有相同的质子数,是氢元素的三种同位素 |
对于可逆反应:A(g)+2B(g)?nC(g),符合如图关系的结论是( )


| A、P1>P2,n<3 |
| B、P1>P2,n>3 |
| C、P1<P2,n>3 |
| D、P1<P2,n<3 |