题目内容
6.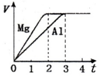 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.反应中镁和铝的( )
| A. | 物质的量之比为3:2 | B. | 质量之比为2:3 | ||
| C. | 摩尔质量之比为2:3 | D. | 反应速率之比为3:2 |
分析 硫酸过量,Mg、Al完全反应,由图可知生成氢气体积相同,则氢气物质的量相等,假设氢气为1mol,根据电子转移守恒计算Mg、Al物质的量,再根据m=nM计算各自质量,进而计算二者物质的量之比、质量之比,摩尔质量之比等于相对分子质量之比,根据v=$\frac{\frac{△n}{V}}{△t}$知,当气体体积相同时,反应速率与其时间成反比.
解答 解:硫酸过量,Mg、Al完全反应,由图可知生成氢气体积相同,则氢气物质的量相等,假设氢气为1mol,根据电子转移守恒,Mg的物质的量为$\frac{1mol×2}{2}$=1mol、Al物质的量为$\frac{1mol×2}{3}$=$\frac{2}{3}$mol.
A.Mg、Al的物质的量之比为1mol:$\frac{2}{3}$mol=3:2,故A正确;
B.Mg、Al的质量之比为1mol×24g/mol:$\frac{2}{3}$mol×27g/mol=4:3,故B错误;
C.Mg、Al的摩尔质量之比为24g/mol:27g/mol=8:9,故C错误;
D.根据v=$\frac{\frac{△n}{V}}{△t}$知,当气体体积相同时,反应速率与其时间成反比,所以二者反应速率之比3:2,故D正确,
故选:AD.
点评 本题以化学反应图象形式,考查化学方程式有关计算,关键是明确金属完全反应且生成氢气的体积相等,注意利用守恒法解答.

练习册系列答案
相关题目
17.除去下列物质中的少量杂质(括号内),选用的试剂和分离方法不能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 粗苯甲酸(泥沙等) | 水 | 重结晶 |
| B | 甲烷(乙烯) | 高锰酸钾酸性溶液 | 洗气 |
| C | 乙炔(硫化氢) | 硫酸铜溶液 | 洗气 |
| D | 溴苯(溴) | 稀氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
14.在pH=13的无色溶液中能大量共存的是( )
| A. | NH4+、SO42-、Cl- | B. | Al3+、N03-、Cl- | C. | K+、MnO4-、SO42- | D. | Na+、CO32-、NO3- |
1.下列测定常温下1mo1氢气体积的操作中,使结果偏大的是( )
| A. | 镁带中混有与酸不反应的杂质 | |
| B. | 装置接口连接处有气体泄漏 | |
| C. | 液体量瓶刻度读数未扣去硫酸的体积 | |
| D. | 硫酸注入量不足,镁带未反应完全 |
11.今有分别含①HSO3-;②两个原子核10e-的阴离子;③SO32-;④HS-;⑤26M2+;⑥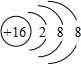 离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
 离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )| A. | ①②④ | B. | ②③⑤ | C. | ①④ | D. | ③⑤⑥ |
3.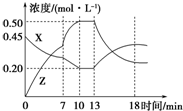 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )| A. | 第7 min时升高温度、第13 min时降低温度 | |
| B. | 第7 min时使用催化剂、第13 min时升高温度 | |
| C. | 第7 min时降低温度、第13 min时增大压强 | |
| D. | 第7 min时减小压强、第13 min时升高温度 |
4.在甲乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-六种离子中的三种,已知乙烧杯中的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )
| A. | Cu2+、H+、Cl- | B. | Cl-、CO32-、OH- | C. | K+、OH-、CO32- | D. | K+、H+、Cl- |
