题目内容
在一定温度下,向一个容积不变的容器中,加入3molSO2和2molO2 及固体催化剂,使之反应.2SO2(g)+O2 (g)?2SO3(g);△H=-196.6kJ/mol.平衡时容器内气体压强为起始时的90%.此时
Ⅰ、加入3molSO2和2molO2 发生反应,达到平衡时,放出的热量为 .
Ⅱ、保持同一反应温度,在相同的容器中,将起始物质的量改为amolSO2、bmolO2、cmolSO3(g),欲使平衡时SO3的体积分数为
,
①达到平衡时,Ⅰ与Ⅱ放出的热量 (填序号).
A、一定相等B、前者一定小C、前者大于或等于后者
②a、b、c必须满足的关系是(一个用a、c表示,另一个用b、c表示) .
③欲使起始时反应表现为向正反应方向进行,a的取值范围是: .
Ⅰ、加入3molSO2和2molO2 发生反应,达到平衡时,放出的热量为
Ⅱ、保持同一反应温度,在相同的容器中,将起始物质的量改为amolSO2、bmolO2、cmolSO3(g),欲使平衡时SO3的体积分数为
| 2 |
| 9 |
①达到平衡时,Ⅰ与Ⅱ放出的热量
A、一定相等B、前者一定小C、前者大于或等于后者
②a、b、c必须满足的关系是(一个用a、c表示,另一个用b、c表示)
③欲使起始时反应表现为向正反应方向进行,a的取值范围是:
考点:化学平衡的计算,等效平衡
专题:化学平衡专题
分析:Ⅰ根据压强之比等于物质的量之比计算平衡时混合气体总的物质的量,再利用差量法计算参加反应的二氧化硫的物质的量,结合热化学方程式计算放出的热量;
Ⅱ①根据Ⅰ计算可知,原平衡时SO3的体积分数为
=
,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数为
,则与原平衡为等效平衡,但c>0,Ⅱ参加反应的物质不如Ⅰ多,据此判断;
②根据等效平衡的思想进行计算;
③欲使起始时反应表现为向正反应方向进行,二氧化硫的物质的量大于平衡时的物质的量,但起始总量不能超过3mol,据此答题;
Ⅱ①根据Ⅰ计算可知,原平衡时SO3的体积分数为
| 1mol |
| 4.5mol |
| 2 |
| 9 |
| 2 |
| 9 |
②根据等效平衡的思想进行计算;
③欲使起始时反应表现为向正反应方向进行,二氧化硫的物质的量大于平衡时的物质的量,但起始总量不能超过3mol,据此答题;
解答:
解:(1)由题意气体压强为起使时的90%,则反应后总的物质的量为起使时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3 物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×
=98.3KJ,
故答案为:98.3KJ;
(2)①原平衡时SO3的体积分数为
=
,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数为
,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数仍为
,则与原平衡为等效平衡,c>0,Ⅱ参加反应的物质不如Ⅰ多,放热就少,故答案为:C;
②平衡时SO3的体积分数仍为
,则与原平衡为等效平衡,
2SO2 +O2 ?2SO3
起始Ⅰ3 2
起始Ⅱa b c
折算后的Ⅱa+c b+c/2 0
根据等平衡的思想有,a+c=3,b+c/2=2
故答案为:a+c=3,b+c/2=2;
③根据Ⅰ中的计算可知,反应达到平衡时,参加反应的二氧化硫为1mol,则平衡时二氧化硫的物质的量为2mol,欲使起始时反应表现为向正反应方向进行,二氧化硫的物质的量大于平衡时的物质的量,但起始总量不能超过3mol,所以有2<a≤3,
故答案为:2<a≤3;
2SO2+O2?2SO3 物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×
| 0.5mol |
| 1mol |
故答案为:98.3KJ;
(2)①原平衡时SO3的体积分数为
| 1mol |
| 4.5mol |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| 9 |
②平衡时SO3的体积分数仍为
| 2 |
| 9 |
2SO2 +O2 ?2SO3
起始Ⅰ3 2
起始Ⅱa b c
折算后的Ⅱa+c b+c/2 0
根据等平衡的思想有,a+c=3,b+c/2=2
故答案为:a+c=3,b+c/2=2;
③根据Ⅰ中的计算可知,反应达到平衡时,参加反应的二氧化硫为1mol,则平衡时二氧化硫的物质的量为2mol,欲使起始时反应表现为向正反应方向进行,二氧化硫的物质的量大于平衡时的物质的量,但起始总量不能超过3mol,所以有2<a≤3,
故答案为:2<a≤3;
点评:本题为化学平衡和反应热综合试题,试题难度较大,注意等效平衡的原理的运用.

练习册系列答案
相关题目
将0.3mol硝酸银、0.6mol硝酸铜、0.7mol氯化钾溶于水,配成100mL溶液,用惰性电极电解一段时间后,若在一极析出0.4mol铜,此时在另一极上产生的气体体积(标准状况)为多少( )
| A、4.48L | B、5.6L |
| C、6.72L | D、8.96L |
一种激素类药物的结构如下,下列有关叙述中不正确的是( )
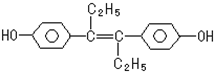

| A、1mol该有机物完全燃烧需要22 mol O2 |
| B、可与NaOH发生反应 |
| C、1mol该有机物可以与7mol Br2发生反应 |
| D、该有机物遇FeCl3溶液呈紫色 |
有关煤的说法正确的是( )
| A、煤中含有单质碳、苯、二甲苯、焦炉气 |
| B、煤的干馏是物理变化 |
| C、煤由复杂的有机物和无机物组成,煤的干馏是化学变化 |
| D、煤主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素 |
下列各组混合物,只要总质量一定,无论它们按什么比例混合,完全燃烧后生成的H2O和CO2都为恒量的是( )
| A、C2H2、C2H6 |
| B、C2H4、C3H8 |
| C、C2H4O、C3H6O |
| D、CH2O、C6H12O6 |
“耐高温长寿命抗氧化陶瓷基复合材料应用技术”获2004午度国家投术发明一等奖.该复合材料的强度比钢还大,在航容航天器中用来替代金属材料,可节约20~30%的燃料.下列关于该材料的叙述中不正确的是( )
| A、该材料属于新型无机非金属材料 |
| B、该材料的化学性质非常稳定 |
| C、与金属一样有较好的传热性能 |
| D、可以替代金属做耐高温结构材料 |