题目内容
常温下,下列叙述正确的是
- A.pH值等于5的HCl溶液和PH值等于9的NaOH溶液由水电离出的C(H+)之比为1:1
- B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
- C.PH=2的HNO3溶液和PH=10的Ba(OH)2溶液等体积混合后的溶液的PH=7
- D.向0.1 mol/L的氨水中加入少量醋酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
A
试题分析:常温下,pH等于5的HCl溶液和pH值等于9的NaOH溶液由水电离出的C(H+)均为10-9mol/L,A正确;c(H+)=c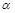 ,酸浓度越大,电离度越小。所以c1>10c2,B错误;pH=2的HNO3溶液和pH=10的Ba(OH)2溶液等体积混合后HNO3过量,pH<7,C错误;氨水中加入醋酸铵固体,平衡向左移动,c(OH-)减小、c(NH3·H2O)增大,c(OH-)/c(NH3·H2O)减小,D错误。
,酸浓度越大,电离度越小。所以c1>10c2,B错误;pH=2的HNO3溶液和pH=10的Ba(OH)2溶液等体积混合后HNO3过量,pH<7,C错误;氨水中加入醋酸铵固体,平衡向左移动,c(OH-)减小、c(NH3·H2O)增大,c(OH-)/c(NH3·H2O)减小,D错误。
考点:水的电离 电离度 pH计算 弱电解质电离平衡
点评:酸、碱抑制水的电离,能水解的盐促进水的电离。
试题分析:常温下,pH等于5的HCl溶液和pH值等于9的NaOH溶液由水电离出的C(H+)均为10-9mol/L,A正确;c(H+)=c
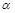 ,酸浓度越大,电离度越小。所以c1>10c2,B错误;pH=2的HNO3溶液和pH=10的Ba(OH)2溶液等体积混合后HNO3过量,pH<7,C错误;氨水中加入醋酸铵固体,平衡向左移动,c(OH-)减小、c(NH3·H2O)增大,c(OH-)/c(NH3·H2O)减小,D错误。
,酸浓度越大,电离度越小。所以c1>10c2,B错误;pH=2的HNO3溶液和pH=10的Ba(OH)2溶液等体积混合后HNO3过量,pH<7,C错误;氨水中加入醋酸铵固体,平衡向左移动,c(OH-)减小、c(NH3·H2O)增大,c(OH-)/c(NH3·H2O)减小,D错误。考点:水的电离 电离度 pH计算 弱电解质电离平衡
点评:酸、碱抑制水的电离,能水解的盐促进水的电离。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
常温下,下列叙述正确的是( )
| A、中和PH和体积均相同的盐酸和硫酸溶液,消耗NaOH的物质的量之比是1:2 | B、在滴有酚酞的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 | C、1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 | D、若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11 |
常温下,下列叙述正确的是( )
| A、PH等于5的HCl溶液和PH值等于9的NaOH溶液由水电离出的C(H+)之比为1:1 | ||
| B、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、PH=2的HNO3溶液和PH=10的Ba(OH)2溶液等体积混合后的溶液的PH=7 | ||
D、向0.1mol/L的氨水中加入少量醋酸铵固体,则溶液中
|