题目内容
7.某同学利用如图1装置探究温度对化学平衡的影响,已知烧瓶中存在如下平衡:2NO2?N2O4△H<0.当进行图2实验后,以下结论正确的是( )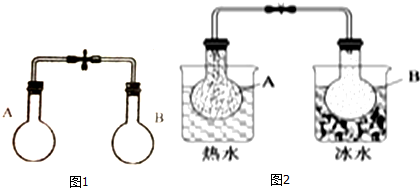
| A. | 图2中,B烧瓶颜色较深 | |
| B. | 图2中,B烧瓶与A烧瓶相比有较多的NO2 | |
| C. | 图2中B烧瓶的正反应速率比图1中B烧瓶的快 | |
| D. | 图2中A烧瓶的正反应速率比图1中A烧瓶的快 |
分析 2NO2(g)?N2O4的正反应是放热反应,升高温度平衡逆向移动,降低温度平衡正向移动,所以图2中A烧瓶颜色加深、B烧瓶颜色变浅;温度升高,反应速率加快,温度降低,反应速率减小,据此进行解答.
解答 解:A.图2中A烧瓶温度升高,则平衡向着逆向移动,导致二氧化氮浓度增大,所以图2中A烧瓶颜色加深,故A错误;
B.图2中,A中温度大于B,在平衡向着逆向移动,所以图2中,、B烧瓶与A烧瓶相比有较少的NO2,故B错误;
C.温度越低,反应速率越慢,则图2中B烧瓶的正反应速率比图1中B烧瓶的慢,故C错误;
D.温度越高,反应速率越快,则图2中A烧瓶的正反应速率比图1中A烧瓶的快,故D正确;
故选D.
点评 本题考查了化学平衡及其影响,题目难度中等,明确温度对化学平衡的影响为解答关键,注意掌握化学平衡及其影响因素,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
17.表是元素周期表的一部分,回答下列问题:
(1)写出①、②两种元素的名称:碳、氮.
(2)写出⑧、⑨两种元素的符号:Si、P.
(3)在这些元素中,最活泼的金属的离子结构示意图是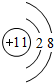 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
(4)这些元素的最高价氧化物对应水化物中,HClO4(填化学式,下同)酸性最强,NaOH的碱性最强;能形成两性氢氧化物的元素是Al(填元素符号).
(5)在⑤到⑪的元素中,Cl(填元素符号)原子半径最小.
(6)比较⑤和⑥的化学性质,Na(填元素符号)更活泼,试用实验证明之(简述操作、现象和结论)金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.
| 族 周期 | IA | IIA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出⑧、⑨两种元素的符号:Si、P.
(3)在这些元素中,最活泼的金属的离子结构示意图是
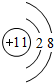 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.(4)这些元素的最高价氧化物对应水化物中,HClO4(填化学式,下同)酸性最强,NaOH的碱性最强;能形成两性氢氧化物的元素是Al(填元素符号).
(5)在⑤到⑪的元素中,Cl(填元素符号)原子半径最小.
(6)比较⑤和⑥的化学性质,Na(填元素符号)更活泼,试用实验证明之(简述操作、现象和结论)金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.
18.某离子的结构示意图为 关于该粒子的说法不正确的是( )
关于该粒子的说法不正确的是( )
 关于该粒子的说法不正确的是( )
关于该粒子的说法不正确的是( )| A. | 核电荷数为17 | B. | 核外有3个电子层 | ||
| C. | 属于非金属元素原子 | D. | 在化学反应中容易失去1个电子 |
15.在固定容积的容器中盛有1molPCl5,200℃时发生如下反应:PCl5(g)?PCl3+Cl2(g)达到平衡时,PCl5体积分数为M%.若恒温下向容器中再通入1molPCl5,再次达平衡时,PCl5所占体积分数为N%,则M和N的关系是( )
| A. | M>N | B. | M<N | C. | M=N | D. | 无法判断 |
12.下列电离方程式正确的是( )
| A. | NH4Cl?NH4++Cl- | B. | H2S?2H++S2- | ||
| C. | KHCO3?K++H+++CO3- | D. | CH3COONH4=NH4++CH3COO- |
19.在含CH3COOH和CH3COONa均为0.1mol/L的溶液中,测得c(CH3COO-)>c(Na+)则下列关系式中正确的是( )
| A. | c(H+)>c(OH-) | B. | c(H+)<c(OH-) | ||
| C. | c(CH3COOH)>c( CH3COO-) | D. | c(CH3COOH)+c(CH3COO- )=0.2mol/L |
16.下列元素中非金属性最强的是( )
| A. | O | B. | F | C. | S | D. | Cl |
17.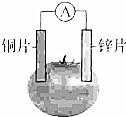 甲乙两位同学一起做水果电池的实验,测得数据如下:
甲乙两位同学一起做水果电池的实验,测得数据如下:
甲同学提出的问题,乙同学解释不正确的是( )
①甲:实验6中负极电极反应式如何写?
乙:铝为负极:Al-3e-=Al3+
②甲:实验1、5中电流方向为什么相反?
乙:实验1中锌比铜活泼,锌为负极,实验5中铝为负极,铝失去电子,电流由锌经导线流向铝
③甲:水果电池的电压与哪些因素有关?
乙:只跟水果的品种有关.
 甲乙两位同学一起做水果电池的实验,测得数据如下:
甲乙两位同学一起做水果电池的实验,测得数据如下:| 试验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
| 2 | 锌 | 铜 | 苹果 | 3 | 650 |
| 3 | 锌 | 铜 | 柑桔 | 3 | 850 |
| 4 | 锌 | 铜 | 西红柿 | 3 | 750 |
| 5 | 锌 | 铝 | 菠萝 | 3 | 650 |
| 6 | 锌 | 铝 | 苹果 | 3 | 450 |
①甲:实验6中负极电极反应式如何写?
乙:铝为负极:Al-3e-=Al3+
②甲:实验1、5中电流方向为什么相反?
乙:实验1中锌比铜活泼,锌为负极,实验5中铝为负极,铝失去电子,电流由锌经导线流向铝
③甲:水果电池的电压与哪些因素有关?
乙:只跟水果的品种有关.
| A. | ③ | B. | ① | C. | ①②③ | D. | ②③ |