题目内容
某探究学习小组做了如下实验:在足量的氯化亚铁溶液中加入1滴液溴,振荡后溶液变为黄色.甲同学认为是Br2单质溶于水形成黄色溶液,而乙同学认为是Fe2+被氧化成Fe3+使溶液变成黄色.
(1)你认为两同学的观点中正确的是 (填“甲”或“乙”),
请你根据提供试剂通过实验验证你的判断:
试剂:A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳
D.硫氰化钾溶液 E.硝酸银溶液
判断:请用原理不同的两种方法加以验证,将选用的试剂编号及实验中观察到的现象填表:
(2)若选用淀粉碘化钾溶液判断两个同学的观点哪个正确,是否可行?若可行,本问不需回答,若不可行请说明原因: ;
(3)若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是 ,该操作的名称是 .
(1)你认为两同学的观点中正确的是
请你根据提供试剂通过实验验证你的判断:
试剂:A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳
D.硫氰化钾溶液 E.硝酸银溶液
判断:请用原理不同的两种方法加以验证,将选用的试剂编号及实验中观察到的现象填表:
| 选用试剂 | 实验现象 | |
| 第一种方法 | ||
| 第二种方法 |
(3)若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是
考点:探究铁离子和亚铁离子的转化
专题:实验探究和数据处理题
分析:(1)溴单质氧化性较强,能将亚铁离子氧化为三价铁,三价铁在水溶液中是黄色的,可以从是否有溴单质以及是否生成三价铁两个角度来设计实验验证;
(2)三价铁和溴单质均能将亚铁离子氧化,碘单质遇到淀粉变蓝;
(3)溴水的分离可以采用萃取法,使用分液漏斗来进行实验.
(2)三价铁和溴单质均能将亚铁离子氧化,碘单质遇到淀粉变蓝;
(3)溴水的分离可以采用萃取法,使用分液漏斗来进行实验.
解答:
解:(1)溴单质氧化性较强,能将亚铁离子氧化为三价铁而使溶液变为黄色,可以进行试验看是否存在溴单质,也可以用硫氰化钾溶液检验三价铁的存在,故答案为:乙;
(2)溴单质也能将碘离子氧化为碘单质,则不可以选用淀粉碘化钾溶液来试验推断是否正确,
故答案为:不可行,因为Br2和Fe3+都能把I-氧化成I2;
(3)向溴水中加入萃取剂可以实现二者的分离,可以选用四氯化碳,四氯化碳和水互不相溶,分层后分液来分离,必须使用分液漏斗,
故答案为:分液漏斗;萃取.
| 选用试剂 | 实验现象 | |
| 第一种方法 | C | 有机层(下层)无色 |
| 第二种方法 | D | 溶液变红 |
故答案为:不可行,因为Br2和Fe3+都能把I-氧化成I2;
(3)向溴水中加入萃取剂可以实现二者的分离,可以选用四氯化碳,四氯化碳和水互不相溶,分层后分液来分离,必须使用分液漏斗,
故答案为:分液漏斗;萃取.
点评:本题是一道关于氧化还原反应的实验设计和探究题,题目难度中等,主要涉及了铁离子、亚铁离子的转化,试题综合性较强,有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
 如图是我国“长征二号F”运载火箭发射现场.图中可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是( )
如图是我国“长征二号F”运载火箭发射现场.图中可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是( )| A、是溴蒸气,火箭发射时作氧化剂 |
| B、是二氧化氮气体,火箭发射时作还原剂 |
| C、是溴蒸气,火箭发射时作还原剂 |
| D、是二氧化氮气体,火箭发射时作氧化剂 |
下列说法中正确的是( )
| A、含有不同种元素的纯净物叫做化合物 |
| B、水溶液中能电离出H+的化合物一定是酸 |
| C、盐中一定含有金属元素 |
| D、含有氧元素的化合物一定是氧化物 |
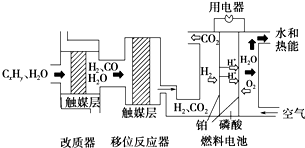 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )| A、该系统中只存在化学能和电能的相互转化 | ||
B、在移位反应器中,反应CO(g)+H2O(g)
| ||
| C、改质器和移位反应器的作用是将CxHy转化为H2和CO2 | ||
| D、该电池正极的电极反应为O2+4H++4e-=2H2O |
溶液和胶体具备的共同性质是( )
| A、分散质微粒都能透过半透膜 |
| B、用石墨电极做导电性实验时,分散质微粒都定向且朝一个方向移动 |
| C、都有丁达尔现象 |
| D、都比较稳定 |
 X、Y、Z、R、W、M五种元素分别位于周期表中四个紧邻的周期,原子序数依次增大,其它相关信息如下列两表所示:
X、Y、Z、R、W、M五种元素分别位于周期表中四个紧邻的周期,原子序数依次增大,其它相关信息如下列两表所示: