题目内容
中国环境监测总站数据显示,颗粒物(PM2.5)是连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据判断PM2.5的酸碱性,试样的pH= .
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图:
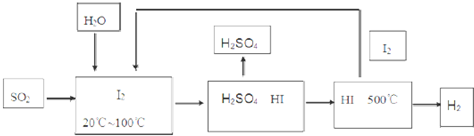
①用离子方程式表示反应器中发生的反应: .
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 .
(1)将PM2.5样本用蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度 /mol.L-1 | 4×10-5 | 6×10-5 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图:

①用离子方程式表示反应器中发生的反应:
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是
考点:常见的生活环境的污染及治理
专题:元素及其化合物,化学应用
分析:(1)根据溶液中电荷守恒计算;
(2)①从流程图可知,在反应器中,I2氧化SO2,生成硫酸和HI;
②HI分解是可逆反应,分离出氢气有利于平衡正向移动.
(2)①从流程图可知,在反应器中,I2氧化SO2,生成硫酸和HI;
②HI分解是可逆反应,分离出氢气有利于平衡正向移动.
解答:
解:(1)溶液中电荷守恒:C(K+)+C(NH4+)+c(Na+)+C(H+)=2C(SO42-)+C(NO3-)+C(Cl-)+c(OH-)和KW,得C(H+)=1×10-4mol?L-1,pH值为4,
故答案为:4;
(2)①从流程图可知,在反应器中,I2氧化SO2,生成硫酸和HI,反应方程式为SO2+I2+2H2O=SO42-+2I-+4H+,故答案为:SO2+I2+2H2O=SO42-+2I-+4H+;
②HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行,故答案为:HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
故答案为:4;
(2)①从流程图可知,在反应器中,I2氧化SO2,生成硫酸和HI,反应方程式为SO2+I2+2H2O=SO42-+2I-+4H+,故答案为:SO2+I2+2H2O=SO42-+2I-+4H+;
②HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行,故答案为:HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
点评:本题考查了电解质溶液中的电荷守恒、反应热=反应物的键能和-生成物的键能和、化学反应自发进行的条件、平衡移动等等知识,题目难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列能说明可逆反应2A(g)+B(g)?2C(g)+D(g)在一定条件下已达到化学平衡状态的事实是( )
| A、容器内压强不随时间的变化而变化 |
| B、容器内A、B、C、D四者共存 |
| C、C的生成速率是D的生成速率的两倍 |
| D、A的消耗速率是D的消耗速率的两倍 |
下列措施或事实不能用勒夏特列原理解释的是( )
| A、新制的氯水在光照下颜色变浅 |
| B、合成NH3反应,为提高NH3的产率,理论上应采取相对较低温度的措施 |
| C、向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 |
| D、实验室中常用排饱和食盐水的方式收集氯气 |
一个原电池的总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的合理组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Cu | Zn | CuSO4 |
| B | Cu | Zn | H2SO4 |
| C | Zn | Cu | CuCl2 |
| D | Mg | Zn | CuCl2 |
| A、A | B、B | C、C | D、D |
常温下,下列各组粒子在指定溶液中能量共存的是( )
| A、在酸性KMnO4溶液中:Na+、C2H5OH、NH4+、Cl- |
| B、能溶解CaCO3的溶液中:Fe2+、Ca2÷、Cl-、NO3- |
| C、澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl- |
| D、能使淀粉-KIO3试纸显蓝色的溶液中:K+、H+、SO42-、I- |
下列对化学反应速率的认识正确的是( )
| A、H+和OH-的反应活化能接近于零,反应几乎在瞬间完成 |
| B、对于任何化学反应来说,反应速率越大,反应现象就越明显 |
| C、选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
| D、化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
下列说法正确的是( )
| A、两种原子形成的共价键一定是极性共价键 |
| B、元素金属性越强,对应单质的还原性越强;元素非金属性越强,对应单质的氧化性越强 |
| C、由金属元素和非金属元素组成的化合物一定是离子化合物 |
| D、按照元素周期表的排布规律,非金属元素最多有23种 |