题目内容
16.下列除杂方案正确的是( )| A. | 氢氧化钠溶液中混有氢氧化钡(硫酸铜溶液) | |
| B. | 二氧化碳气体中混有氯化氢(氢氧化钠溶液) | |
| C. | 硝酸铜溶液中混有硝酸银(铜粉) | |
| D. | 氧化钙中混有碳酸钠(稀盐酸) |
分析 A.氢氧化钡与硫酸铜反应生成沉淀,NaOH与硫酸铜反应生成沉淀;
B.二者均与NaOH反应;
C.Cu与硝酸银反应生成硝酸铜和Ag;
D.二者均与稀盐酸反应.
解答 解:A.二者均与硫酸铜溶液反应,不能除杂,故A错误;
B.二者均与NaOH反应,不能除杂,故B错误;
C.Cu与硝酸银反应生成硝酸铜和Ag,则反应后过滤可除杂,故C正确;
D.二者均与稀盐酸反应,不能除杂,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
18.粗盐提纯实验中要除去Ca2+、Mg2+等离子,不使用的试剂是( )
| A. | 硫酸 | B. | 纯碱 | C. | 烧碱 | D. | 盐酸 |
4.已知1L溶液中已电离的水是10-10mol,在此溶液中肯定能大量共存的离子组是( )
| A. | K+、Na+、NO3-、SO42- | B. | CO32-、Cl-、K+、Na+ | ||
| C. | Mg2+、NO3-、Cl-、K+ | D. | NO3-、NH4+、K+、SO42- |
11.蒸馏时温度计的水银球应处在什么位置( )
| A. | 液面下 | B. | 液面上 | ||
| C. | 蒸馏烧瓶支管口 | D. | 蒸馏烧瓶中任何位置 |
1.常温下,某溶液中水电离产生的c(H+)=1×10-12mol/L,该溶液中一定能大量共存的离子组是( )
| A. | K+、Na+、HSO3-、Cl- | B. | Na+、Ba2+、NO3-、Cl- | ||
| C. | K+、S2-、Cl-、CO32- | D. | K+、NH4+、Cl-、SO42- |
5.把铝片放入盛有过量稀硫酸的试管中,下列措施不能加快产生氢气的速率的是( )
| A. | 把稀硫酸换为浓硫酸 | B. | 把铝片换成镁片 | ||
| C. | 加入少量CuSO4溶液 | D. | 加少量NaHSO4固体 |
6.下列有关甲苯的说法中,不正确的是( )
| A. | 可以与溴水发生取代反应 | B. | 可以与氢气发生加成反应 | ||
| C. | 可以制造烈性炸药TNT | D. | 可以被酸性高锰酸钾溶液氧化 |
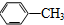 E.
E.