题目内容
6.下列有关物质的量浓度的相关说法中正确的是( )| A. | 将25gCuSO4.5H2O晶体加水配成100mL溶液,该溶液的物质的量浓度为1mol/L | |
| B. | 将100mL5mol/L盐酸溶液在蒸发皿中蒸发至50mL溶液,物质的量浓度变为10mol/L | |
| C. | 0.3mol/L的Na2SO4溶液中含有的Na+和SO42- 的总物质的量为0.9mol | |
| D. | 实验室要用容量瓶配制0.2mol/L的NaCl溶液950mL,应称量NaCl固体11.1g |
分析 A.计算硫酸铜晶体物质的量n=$\frac{m}{M}$,溶质物质的量难度c=$\frac{n}{V}$计算分析;
B.盐酸溶液中氯化氢易挥发;
C.溶液体积不知不能计算溶液中微粒数;
D.配制0.2mol/L的NaCl溶液950mL,容量瓶无此规格,应配制1000ml,0.2mol/L的溶液,量取出950mL.
解答 解:A.将25gCuSO4.5H2O晶体,物质的量n=$\frac{25g}{250g/mol}$=0.1mol,加水配成100mL溶液,该溶液的物质的量浓度=$\frac{0.1mol}{0..1L}$=1mol/L,故A正确;
B.将100mL5mol/L盐酸溶液在蒸发皿中蒸发至50mL溶液,溶液中氯化氢挥发,得不到物质的量浓度10mol/L的溶液,故B错误;
C.0.3mol/L的Na2SO4溶液体积不知不能计算微粒数,故C错误;
D.配制0.2mol/L的NaCl溶液950mL,容量瓶无此规格,应配制1000ml,0.2mol/L的溶液,称量氯化钠质量=0.2mol/L×1L×58.5g/mol=11.7g,故D错误;
故选A.
点评 本题考查了物质的量浓度概念、溶液配制方法,注意物质的量和各物理量的计算关系和容量瓶的选择,题目难度中等.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
16.下列说法正确的是( )
| A. | 相同温度下,硫酸溶液的导电能力应强于醋酸溶液的导电能力 | |
| B. | NaCl在电流作用下电离成Na+和Cl- | |
| C. | CuSO4溶液导电时要伴随化学变化 | |
| D. | CO2水溶液的导电能力较弱,CO2是弱电解质 |
14.在无色溶液中,下列各组离子可能大量共存的是( )
| A. | OH-、NO3-、HCO3-、Na+ | B. | Na+、SO42-、Mg2+、I- | ||
| C. | NO3-、Cu2+、K+、Cl- | D. | H+、K+、ClO-、Ba2+ |
1.根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | Ka=3×10-8 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 |
| A. | c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) | B. | c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) | ||
| C. | c(HCO3-)>c(ClO-)>c(OH-) | D. | c(ClO-)>c(HCO3-)>c(H+) |
18.实验室里坩埚的材质种类很多,可以用于熔融烧碱的坩埚是( )
| A. | 普通玻璃坩埚 | B. | 铁坩埚 | C. | 石英坩埚 | D. | 陶瓷坩埚 |
15. 某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:
某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:
(1)用物质的A表示的反应的平均速率为0.3mol/L•s.
(2)2s时物质A的转化率为30%.
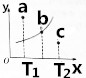
(3)图中的曲线是该反应在不同温度下的平衡曲线,x中表示温度,y轴表示B的转化率,图中有a、b、c三点,
①该反应是吸热(填“吸热”或“放热”)反应;
②C点:v正>v逆(填“>”、“<”或“=”).
(4)一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入A和B,其起始物质的量及A的平衡转化率如下表所示:
①该温度下,乙中反应的平衡常数K为400;
②A的平衡转化率:α2>α1(填“>”、“<”或“=”);
③容器中C的物质的量浓度:甲<丁(填“>”、“<”或“=”).
 某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:
某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:| 密闭容器 | A | B | C |
| n(起始状态)/mol | 4 | 2 | 0 |
| n(平衡状态)/mol | 2.8 | 1.4 | 1.2 |
(2)2s时物质A的转化率为30%.
(3)图中的曲线是该反应在不同温度下的平衡曲线,x中表示温度,y轴表示B的转化率,图中有a、b、c三点,
①该反应是吸热(填“吸热”或“放热”)反应;
②C点:v正>v逆(填“>”、“<”或“=”).
(4)一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入A和B,其起始物质的量及A的平衡转化率如下表所示:
| 密闭容器 | 甲 | 乙 | 丙 | 丁 | |
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(A)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(B)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| A的平衡转化率 | 80 | α1 | α2 | α3 | |
②A的平衡转化率:α2>α1(填“>”、“<”或“=”);
③容器中C的物质的量浓度:甲<丁(填“>”、“<”或“=”).
16.下列元素-定为主族元素的是( )
| A. | 其原子最外电子层有7个电子的元素 | |
| B. | 最高正价为+3的元素 | |
| C. | 其原子最外层电子数大于电子层的元素 | |
| D. | 最高价氧化物对应的水化物是酸的元素 |
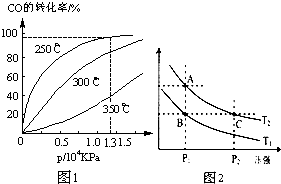 工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇: