题目内容
X和Y两种元素可以形成XY2型化合物,则X和Y的原子序数为( )
| A、3和9 | B、6和8 |
| C、7和12 | D、10和14 |
考点:位置结构性质的相互关系应用
专题:化学键与晶体结构
分析:短周期非金属元素X和Y能形成XY2型化合物,若X、Y的化合价分别为+2、-1价时,X处于ⅡA、Y处于ⅦA(或Y为H),还可能有SCl2等;若X、Y的化合价分别为+4、-2价时,X处于ⅣA、Y处于ⅥA,还有可能为SO2、NO2等,据此解答.
解答:
解:A.X和Y的原子序数为3和9,分别为Li和F,形成化合物为LiF,故A错误;
B.X和Y的原子序数为6和8,分别为C和O,形成化合物为CO2,故B正确;
C.X和Y的原子序数为7和12,分别为N和Mg,形成化合物为Mg3N2,故C错误;
D.X和Y的原子序数为10和14,分别为Ne和Si,二者不反应,故D错误.
故选B.
B.X和Y的原子序数为6和8,分别为C和O,形成化合物为CO2,故B正确;
C.X和Y的原子序数为7和12,分别为N和Mg,形成化合物为Mg3N2,故C错误;
D.X和Y的原子序数为10和14,分别为Ne和Si,二者不反应,故D错误.
故选B.
点评:本题考查结构性质位置关系,为高频考点,侧重于学生的分析能力的考查,难度中等,注意利用化合价来分析元素在周期表中的位置,注意利用列举法进行的解答.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
下列说法正确的是( )
| A、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 |
| B、使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干 |
| C、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| D、用10mL量筒量取9.2mL NaCl溶液 |
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述不正确的是( )
| A、电解时以精铜作阴极 |
| B、电解时阴极发生还原反应 |
| C、粗铜连接电源负极,其电极反应有:Cu-2e-=Cu2+、Fe-2e-=Fe2+、Zn-2e-=Zn2+ |
| D、电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
利用下列实验装置能完成相应实验的是( )
A、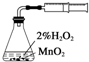 测定化学反应速率 |
B、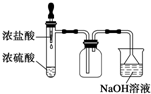 制取并吸收Cl2 |
C、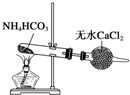 制备纯净的NH3 |
D、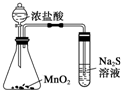 比较MnO2、Cl2、S的氧化性 |
下列各式中,属于水解方程式的是( )
| A、HCO3-+OH-=H2O+CO32- |
| B、NH3+H+=NH4+ |
| C、NH3?H2O?NH4++OH- |
| D、HCO3-+H2O?H2CO3+OH- |
下列除杂质的操作中不正确的是( )
| A、NaHCO3溶液中混有少量Na2CO3:往该溶液中加入过量Ca(HCO3)2溶液 |
| B、CO2中混有HCl:将其通入饱和NaHCO3溶液 |
| C、铁粉中混有铝粉:加入过量烧碱溶液充分反应、过滤 |
| D、NaCl固体中混有少量I2:充分加热 |
 A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答: