题目内容
下列事实不能用电化学理论解释的是( )
| A、轮船水线以下的船壳上装一定数量的锌块 |
| B、铁可以在氯气中燃烧 |
| C、纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
| D、镀锌的铁比镀锡的铁耐用 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:不能用电化学原理解释说明该装置不能构成原电池,只能发生化学腐蚀,根据原电池的构成条件来分析解答,原电池的构成条件是:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,作原电池负极的金属加速被腐蚀,作原电池正极的金属被保护.
解答:
解:A.锌、铁和电解质溶液能构成原电池,锌易失电子作负极,铁作正极,所以能用电化学原理解释,故A不选;
B.铁在氯气中燃烧,铁与氯气发生化学反应,没构成原电池,不能用原电池原理解释,故B选;
C.锌置换出铜,锌、铜和电解质溶液能构成原电池,反应速率加快,锌易失电子作负极,铜作正极,所以能用电化学原理解释,故C不选;
D.ZnFe构成原电池时,Zn活泼作负极被腐蚀,Fe被保护,镀锡的铁破损后,Fe活泼,被腐蚀,所以能用电化学原理解释,故D不选;
故选B.
B.铁在氯气中燃烧,铁与氯气发生化学反应,没构成原电池,不能用原电池原理解释,故B选;
C.锌置换出铜,锌、铜和电解质溶液能构成原电池,反应速率加快,锌易失电子作负极,铜作正极,所以能用电化学原理解释,故C不选;
D.ZnFe构成原电池时,Zn活泼作负极被腐蚀,Fe被保护,镀锡的铁破损后,Fe活泼,被腐蚀,所以能用电化学原理解释,故D不选;
故选B.
点评:本题考查了金属的腐蚀与防护,明确电化学腐蚀与化学腐蚀的区别是解本题关键,再结合原电池构成条件来分析解答,难度不大.

练习册系列答案
相关题目
基态原子的核外电子排布为[Kr]4d55s2的元素属于的区、周期和族为( )
| A、p区、第五周期、ⅠB族 |
| B、d区、第五周期、ⅦB族 |
| C、d区、第四周期、ⅠB族 |
| D、ds区、第五周期、ⅠB族 |
下列说法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、HCl和NaOH反应中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| D、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ?mol-1 |
用铝箔包裹着2.3克金属钠投入到足量水中,理论上可以收集到氢气物质的量为( )
| A、0.05mol |
| B、0.2mol |
| C、大于0.05mol小于等于0.2mol |
| D、无法判断 |

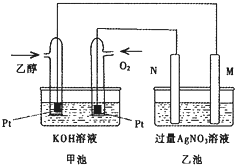 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: