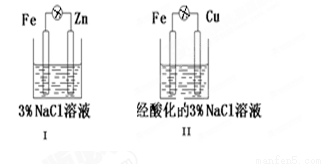
题目内容
下列生活中的化学事例对应的离子方程式书写正确的是
A.用醋酸除去暖瓶中的水垢:2H++CaCO3== Ca2++ CO2↑+ H2O
B.利用Na2CO3溶液可除油污:CO32- + 2H2O  H2CO3 + 2OH-
H2CO3 + 2OH-
C.氢氧燃料电池在酸性介质中的正极反应:O2 +4e- +2H2O = 4OH-
D.汽车用的铅蓄电池充电时阳极反应:PbSO4+2H2O-2e-== PbO2+4H++SO
D
【解析】
试题分析:A、醋酸为弱酸,不能拆成离子,故A错误;B、CO32?的水解反应要分步进行,故B错误;C、在酸性介质中反应,不可能生成OH?,故C错误;D、蓄电池充电时阳极反应,PbSO4失去电子,电极方程式为:PbSO4+2H2O-2e-== PbO2+4H++SO,故D正确。
考点:本题考查离子方程式。

 口算题天天练系列答案
口算题天天练系列答案下列叙述的理由与结论因果关系正确的是
选项 | 理由 | 结论 |
A | 与盐酸反应时,相同物质的量的原子失去电子的数目:Al>Na | 还原性:Al>Na |
B | 室温时,相同物质的量浓度溶液的pH:AlCl3<MgCl2 | 碱性:Mg(OH)2>Al(OH)3 |
C | 相同数目的分子可电离的H+数:H2SO4>HClO4 | 酸性:H2SO4>HClO4 |
D | 用饱和NaHCO3溶液可以除去CO2 中含有的少量SO2 | 非金属性:S > C |
下列实验“操作和现象”与“目的或结论”对应关系正确的是
| 操作和现象 | 目的或结论 |
A | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
B | 向铁和稀硝酸反应后的溶液中若滴加KSCN溶液显红色;若滴加酸性高锰酸钾溶液紫红色褪去 | 该溶液中既有Fe3+,还有Fe2+ |
C | 将铁插入硫酸铜溶液中 | 比较Cu、Fe2+的还原性 |
D | 将产生的气体依次通过无水CuSO4、澄清石灰水和品红溶液 | 检验碳与浓硫酸反应后的气体产物 |
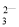 、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是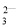
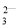 、OH-、Cl-
、OH-、Cl-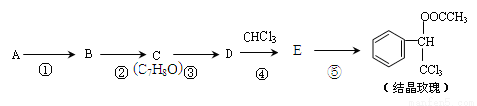
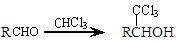 (-R表示烃基)
(-R表示烃基)