题目内容
写出以下化学反应的方程式并按要求分类:
①铁丝在纯氧中燃烧
②氢氧化铝药物治疗胃酸过多:
③氢氧化钠溶液吸收少量二氧化硫气体:
④其中属于氧化还原反应的是 .
①铁丝在纯氧中燃烧
②氢氧化铝药物治疗胃酸过多:
③氢氧化钠溶液吸收少量二氧化硫气体:
④其中属于氧化还原反应的是
考点:氧化还原反应,化学方程式的书写
专题:氧化还原反应专题
分析:①铁丝在纯氧中燃烧生成四氧化三铁,为氧化还原反应;
②氢氧化铝药物治疗胃酸过多,属于复分解反应;
③氢氧化钠溶液吸收少量二氧化硫气体生成亚硫酸钠,不是氧化还原反应;
④有元素化合价变化的反应为氧化还原反应.
②氢氧化铝药物治疗胃酸过多,属于复分解反应;
③氢氧化钠溶液吸收少量二氧化硫气体生成亚硫酸钠,不是氧化还原反应;
④有元素化合价变化的反应为氧化还原反应.
解答:
解:①铁丝在纯氧中燃烧生成四氧化三铁,反应的方程式为3Fe+2O2
Fe3O4,为氧化还原反应,
故答案为:3Fe+2O2
Fe3O4;
②氢氧化铝药物治疗胃酸过多,反应的方程式为Al(OH)3+3HCl═AlCl3+3H2O,
故答案为:Al(OH)3+3HCl═AlCl3+3H2O;
③氢氧化钠溶液吸收少量二氧化硫气体生成亚硫酸钠,反应的方程式为2NaOH+SO2═Na2SO3+H2O,
故答案为:2NaOH+SO2═Na2SO3+H2O;
④以上分析中只有①为氧化还原反应,
故答案为:①.
| ||
故答案为:3Fe+2O2
| ||
②氢氧化铝药物治疗胃酸过多,反应的方程式为Al(OH)3+3HCl═AlCl3+3H2O,
故答案为:Al(OH)3+3HCl═AlCl3+3H2O;
③氢氧化钠溶液吸收少量二氧化硫气体生成亚硫酸钠,反应的方程式为2NaOH+SO2═Na2SO3+H2O,
故答案为:2NaOH+SO2═Na2SO3+H2O;
④以上分析中只有①为氧化还原反应,
故答案为:①.
点评:本题考查氧化还原反应,为高考常见题型,侧重于学生的分析能力的考查,注意从元素化合价变化的角度认识氧化还原反应的概念和物质具有的性质,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
设NA代表阿佛加德罗常数,下列说法正确的是( )
| A、62 g Na2O与78gNa2O2中所含阴离子的个数比为1:2 |
| B、质量相等的两份气体,一份是SO2,另一份是SO3,这两份气体中,SO2与SO3所含氧原子个数之比是6:5 |
| C、在标准状况下,0.5NA个水分子所占体积是11.2 L |
| D、500 mL 1 mol/L Fe2(SO4)3溶液,同250 mL 3 mol/L的Na2SO4溶液所含硫酸根离子的物质的量浓度之比为1:1 |
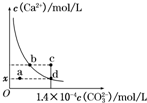 室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )
室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )| A、x数值为2×10-5 |
| B、c点时有碳酸钙沉淀生成 |
| C、加入蒸馏水可使溶液由d点变到a点 |
| D、b点与d点对应的溶度积相等 |
下列关于阿伏加德罗常数NA的说法正确的是( )
| A、1mol/L的NaCl溶液中Na+为NA个 |
| B、1mol水中H原子为2NA个 |
| C、1mol N2H4分子中N和H原子都为NA个 |
| D、2g H2中含NA个电子 |
盐酸具有的化学性质是( )
| A、只有还原性 |
| B、只有酸性 |
| C、只有氧化性 |
| D、有酸性、氧化性、还原性 |

 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.