题目内容
6.下列离子方程式正确的是( )| A. | FeCl3溶液中加入过量的氨水:Fe3++3OH-→Fe(OH)3↓ | |
| B. | AlCl3溶液中加入过量的氨水:Al3++4OH-→AlO2-+2H2O | |
| C. | 金属铁与过量的稀盐酸反应:2Fe+6H+→2Fe3++3H2↑ | |
| D. | 氧化铝与氢氧化钠溶液反应:Al2O3+2OH-→2AlO2-+H2O |
分析 A.一水合氨为弱碱,离子方程式中不能拆开;
B.氨水为弱碱,二者反应生成氢氧化铝沉淀;
C.铁与稀盐酸反应生成的是亚铁离子;
D.氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水.
解答 解:A.氨水为弱碱,一水合氨需要保留分子式,正确的离子方程式为:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,故A错误;
B.氨水碱性较弱,不能弱碱氢氧化铝,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.金属铁与过量的稀盐酸反应生成氯化亚铁和氢气,正确的离子方程式为:Fe+2H+→Fe2++H2↑,故C错误;
D.氧化铝为两性氧化物,氧化铝与氢氧化钠溶液反应的离子方程式为:Al2O3+2OH-→2AlO2-+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.将SO2气体通入BaCl2溶液至饱和,无沉淀生成,再通入气体甲有白色沉淀生成,则气体甲可能是( )
| A. | NO | B. | NH3 | C. | CO2 | D. | HCl |
14.从柑橘中可提炼出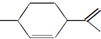 .下列关于它的说法不正确的是( )
.下列关于它的说法不正确的是( )
 .下列关于它的说法不正确的是( )
.下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | |
| B. | 1mol该有机物能与4mol H2发生加成反应 | |
| C. | 能与溴水发生加成反应 | |
| D. | 常温下呈液态,难溶于水 |
1.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z为地壳中含量最高的金属元素.下列说法正确的是( )
| X | ||||||
| Y | Z | W |
| A. | 工业上电解YW饱和溶液冶炼金属Y | |
| B. | 气态氢化物的稳定性:W>X | |
| C. | Y、W的最高价氧化物的水化物均能溶解金属Z | |
| D. | 简单离子半径的大小顺序:r(Y+)>r(X-) |
11.下列物质中,不属于烃类的是( )
| A. | C6H6 | B. | C2H6 | C. | C2H4 | D. | C6H5OH |
18.不粘锅的内壁有一薄层,为聚四氟乙烯.用不粘锅烹烧饭菜是不易粘锅烧焦.下列关于聚四氟乙烯的说法正确的是( )
| A. | 聚四氟乙烯分子中含有双键 | |
| B. | 聚四氟乙烯的单体是不饱和烃 | |
| C. | 聚四氟乙烯的化学性质很稳定,正常使用时不会发生化学变化 | |
| D. | 聚四氟乙烯中的氟的质量分数约为76% |
16.从海水中提取下列物质,可以不涉及化学变化的是( )
| A. | Mg | B. | Br2 | C. | NaCl | D. | K |