题目内容
4.下列变化不能用勒夏特列原理解释的是( )| A. | 红棕色的NO2气体加压后颜色先变深再变浅 | |
| B. | 实验室中常用饱和食盐水除去Cl2中混有的HCl | |
| C. | 二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 | |
| D. | H2、I2、HI混合气体加压后颜色变深 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动;使用勒夏特列原理时,研究对象必须为可逆反应,否则勒夏特列原理不适用;催化剂只能改变反应速率,不会影响化学平衡,所以不能用勒夏特列原理解释.
解答 解:A、可以可逆反应2NO2(g)?N2O4(g),正反应为体积缩小的反应,加压后二氧化氮的浓度增大,所以气体有色加深,由于增大了压强,平衡向生成四氧化二氮的方向移动,故加压后颜色先变深后变浅,可以平衡移动原理解释,故A错误;
B、实验室可用排饱和食盐水的方法收集氯气,氯气和水的反应是可逆反应,饱和氯化钠溶液中氯离子浓度大,化学平衡逆向进行,减小氯气溶解度,能用勒沙特列原理解释,故B错误;
C、工业上生产硫酸存在平衡2SO2+O2?2SO3,使用过量的空气,增大氧气的浓度,平衡向正反应移动,可以提高二氧化硫的利用率,能用勒夏特列原理解释,故C错误;
D、气体两边的计量数相等,增加压强平衡不移动,不能利用勒夏特列原理解释,故D正确;
故选D.
点评 本题考查勒夏特列原理知识,题目难度不大,注意使用勒夏特列原理的前提必须是可逆反应,且是否发生平衡的移动.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
15.下列物质中含有离子键的是( )
| A. | H2O | B. | MgCl2 | C. | CO2 | D. | N2 |
12.下列说法正确的是( )
| A. | 周期表中金属与非金属交界处可找到合成催化剂的元素 | |
| B. | 有热量放出的变化一定是放热反应 | |
| C. | 化学反应中能量变化的主要原因是有化学键的断裂与形成 | |
| D. | 影响化学反应速率的本质因素是催化剂 |
19.已知2H→H2放出437.6kJ的热量,下列说法正确的是( )
| A. | 氢气分子内每个氢原子都达到了8电子稳定结构 | |
| B. | 1molH2的能量比2molH的能量低 | |
| C. | 1molH2离解成2molH要放出437.6kJ的热量 | |
| D. | 氢原子不如氢气分子活泼 |
9.下列有关说法不正确的是( )
| A. | 油脂在碱性条件下水解又可称为皂化反应 | |
| B. | 甲醛和硫酸铵溶液均能使蛋白质变性 | |
| C. | 标准状况下,22.4 L乙烯质量为28 g | |
| D. | 1 mol 甲基所含电子数为9NA |
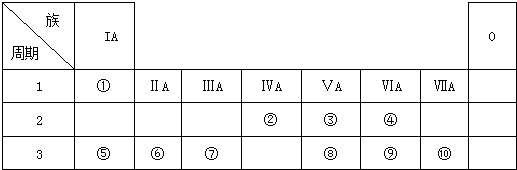
13.下列有关原子结构和元素周期律的表述正确的是( )
| A. | 同周期非金属元素的氧化物对应的水化物的酸性从左到右依次增强 | |
| B. | 第ⅠA 族元素的金属性比第ⅡA 族元素的金属性强 | |
| C. | ⅦA族元素是同周期中非金属性最强的元素 | |
| D. | 原子序数为15的元素的最高化合价为+3 |
14.某药物丙可由有机物甲和乙在一定条件下反应制得
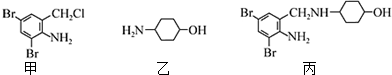
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 甲、乙和丙都属于芳香族化合物 | |
| B. | 乙能与盐酸反应但不能与NaOH溶液反应 | |
| C. | 丙是由甲和乙通过加成反应制得的 | |
| D. | 丙中的两个六元环上的碳原子有可能共平面 |
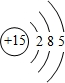 ;
;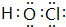
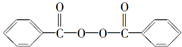
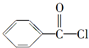 )和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:
)和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式: ,该反应属于取代反应.
,该反应属于取代反应.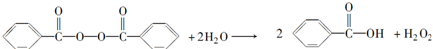 .苯甲酸的同分异构体中,含苯环且属于酯类的结构简式为
.苯甲酸的同分异构体中,含苯环且属于酯类的结构简式为 ,属于酚类结构的同分异构体有3种.
,属于酚类结构的同分异构体有3种.