题目内容
(1)实验室在配制氯化铁溶液时,常出现少许浑浊,原因离子方程式表示为 .为防止出现这样的现象,在配制时常加入
(2)根据下列2个热化学反应方程式:
FeO(s)+CO(g)=Fe(s)+CO2(g)△H=-218kJ/mol
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学反应方程式:
(3)常温下,等物质的量的浓度的①氨水 ②NH4HSO4 ③NH4Cl ④(NH4)2CO3⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为 (填序号)
(2)根据下列2个热化学反应方程式:
FeO(s)+CO(g)=Fe(s)+CO2(g)△H=-218kJ/mol
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学反应方程式:
(3)常温下,等物质的量的浓度的①氨水 ②NH4HSO4 ③NH4Cl ④(NH4)2CO3⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为
考点:盐类水解的应用,用盖斯定律进行有关反应热的计算,盐类水解的原理
专题:
分析:(1)氯化铁为强酸弱碱盐,水解生成氢氧化铁和盐酸,溶液成酸性;
(2)CO气体还原Fe3O4固体得到Fe固体和CO2气体,反应的方程式为4CO(g)+Fe3O4(s)=3Fe(s)+4CO2(g),结合盖斯定律解答;
(3)①是弱碱,部分电离,存在电离过程;②③④⑤都是铵盐是强电解质完全电离,存在水解过程,依据弱电解质的电离和盐类水解平衡移动的影响因素解答.
(2)CO气体还原Fe3O4固体得到Fe固体和CO2气体,反应的方程式为4CO(g)+Fe3O4(s)=3Fe(s)+4CO2(g),结合盖斯定律解答;
(3)①是弱碱,部分电离,存在电离过程;②③④⑤都是铵盐是强电解质完全电离,存在水解过程,依据弱电解质的电离和盐类水解平衡移动的影响因素解答.
解答:
解:(1)氯化铁为强酸弱碱盐,水解呈酸性,水解离子方程式为Fe3++3H2O≒Fe(OH)3+3H+,配制溶液时应防止水解生成沉淀而使溶液变浑浊,则应加入盐酸,
故答案为:Fe3++3H2O?Fe(OH)3+3H+;盐酸;
(2)已知①FeO(s)+CO(g)=Fe(s)+CO2(g)△H=-218kJ/mol,
②Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol,
依据盖斯定律计算②+①×3得到:4CO(g)+Fe3O4(s)=3Fe(s)+4CO2(g)△H=-13.5KJ/moL,
故答案为:4CO(g)+Fe3O4(s)=3Fe(s)+4CO2(g)△H=-13.5kJ/moL;
(3)假设各种溶液的浓度均为1mol/L,②③④⑤都是铵盐是强电解质完全电离,④⑤电离产生的铵根离子浓度约为2mol/L,④碳酸根离子和铵根离子发生双水解相互促进,所以⑤>④;②③电离产生的铵根离子的浓度约为1mol/L,②中硫酸氢根电离产生的氢离子抑制铵根离子的水解,所以②>③;①是弱电解质只有小部分电离,铵根离子浓度远远小于1mol/L,所以铵根离子浓度由大到小的顺序是:⑤>④>②>③>①,
故答案为:⑤④②③①.
故答案为:Fe3++3H2O?Fe(OH)3+3H+;盐酸;
(2)已知①FeO(s)+CO(g)=Fe(s)+CO2(g)△H=-218kJ/mol,
②Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol,
依据盖斯定律计算②+①×3得到:4CO(g)+Fe3O4(s)=3Fe(s)+4CO2(g)△H=-13.5KJ/moL,
故答案为:4CO(g)+Fe3O4(s)=3Fe(s)+4CO2(g)△H=-13.5kJ/moL;
(3)假设各种溶液的浓度均为1mol/L,②③④⑤都是铵盐是强电解质完全电离,④⑤电离产生的铵根离子浓度约为2mol/L,④碳酸根离子和铵根离子发生双水解相互促进,所以⑤>④;②③电离产生的铵根离子的浓度约为1mol/L,②中硫酸氢根电离产生的氢离子抑制铵根离子的水解,所以②>③;①是弱电解质只有小部分电离,铵根离子浓度远远小于1mol/L,所以铵根离子浓度由大到小的顺序是:⑤>④>②>③>①,
故答案为:⑤④②③①.
点评:本题考查盐类水解的应用,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意盐类水解的原理是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
某有机物的结构简式为: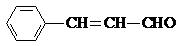 ,则关于该有机物的说法正确的是( )
,则关于该有机物的说法正确的是( )
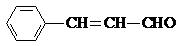 ,则关于该有机物的说法正确的是( )
,则关于该有机物的说法正确的是( )| A、1 mol该有机物发生银镜反应能生成 1 mol Ag |
| B、1 mol该有机物最多能够与6 mol H2 发生加成反应 |
C、它与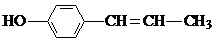 互为同分异构体 互为同分异构体 |
| D、该有机物能被酸性高锰酸钾溶液氧化 |
下列各组中的离子能在pH=1的无色溶液中大量共存的是( )
| A、Ba2+、Na+、I-、ClO- |
| B、Mg2+、Cl-、Al3+、NO3- |
| C、K+、Fe2+、Cl-、MnO4- |
| D、Ca2+、Na+、Fe3+、Br- |
下列每组中各有三对物质,他们都能用分液漏斗分离的是( )
| A、乙酸乙酯和水,酒精和水,植物油和水 |
| B、四氯化碳和水,溴苯和水,硝基苯和水 |
| C、甘油和水,乙酸和水,乙酸和乙醇 |
| D、酒精和水,苯和水,己烷和水 |
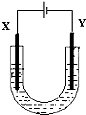 如图是用石墨和铁作电极电解饱和食盐水的装置,请填空:
如图是用石墨和铁作电极电解饱和食盐水的装置,请填空: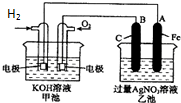 如图是一个化学过程的示意图.已知甲池的总反应式为:2H2+O2═2H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2H2+O2═2H2O
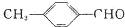 中的含氧官能团,请写出该反应的化学方程式:
中的含氧官能团,请写出该反应的化学方程式: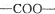 结构的基团
结构的基团