题目内容
12.配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容偏大.分析 分析不当操作对溶质的物质的量和溶液体积的影响,依据c=$\frac{n}{V}$进行误差分析.
解答 解:配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容,氢氧化钠溶解放出热量,溶液有热胀冷缩性质,会导致配制溶液体积偏小,浓度偏大,故答案为:偏大.
点评 本题考查误差分析,侧重考查学生分析判断能力,明确配制原理和过程是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.向27.2gCu和Cu20的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(N03)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性.金属离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
| A. | Cu与Cu20的物质的量之比为2:1 | |
| B. | 硝酸的物质的量浓度为2.4mol/L | |
| C. | 产生的NO在标准状况下的体枳为4.48L | |
| D. | Cu、Cu20与硝酸反应后剩余HN03为lmol |
3.在l01kPa时燃烧1t含FeS2质量分数为70%的黄铁矿(杂质不参加反应)生成固态Fe2O3和气 态SO2,放出4.98×106kJ的热量.表示上述反应的热化学方程式正确的是( )
| A. | 4FeS2( s)+11O2( g)═2Fe2O3( s)+8SO2(g)△H=-3414.8kJ•moL | |
| B. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=-853.7kJ•moL | |
| C. | 4FeS2(s)+11O2(g)═2 Fe2O3 (s)+8SO2(g)△H+3414.8kJ•moL | |
| D. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=+853.7kJ•moL |
7.下列溶液一定呈中性的是( )
| A. | c(H+)=1×10-7 mol/L | B. | c(OH-)=1×10-7mol/L | ||
| C. | c(H+)=c(OH-) | D. | pH=7 |
17.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=(+283.0kJ/mol)×2 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
4.某元素的最外层电子数只有2个,则该元素( )
| A. | 一定是主族元素 | B. | 一定是金属元素 | ||
| C. | 一定是非金属元素 | D. | 可能是金属元素,也可能不是 |
1.下列事实不能用勒夏特列原理解释的是( )
| A. | 高压有利于氨的合成 | |
| B. | 向含有酚酞的氨水溶液中,加入少量NH4Cl晶体,溶液红色变浅 | |
| C. | 常温下,0.1 mol•L-1的盐酸中,由水产生的c(H+)<1.0×10-7mol•L-1 | |
| D. | 使用催化剂可加快SO2转化为SO3的反应速率 |
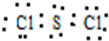 .
.