题目内容
19.运用所学知识,回答下列问题.(1)S原子的价电子排布图为
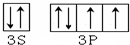 .
.(2)与SCN-互为等电子体的分子有N2O和CO2(任写一种)
(3)SO3的三聚体环状结构如图1所示,该结构中S原子的杂化轨道类型为sp3;该结构中S与O形成的共价键的键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为a(填图中字母的a或b),该分子中含有12个σ键.
(4)化合物Na2O,其晶胞结构如图2所示,晶胞参数,a=0.566nm,晶胞中O原子的配位数为8;列式计算该晶体的密度2.27g•cm-3.(列出计算式即可)

分析 (1)硫是16号元素,有6个价电子,根据核外电子排布规律书写电子排布图;
(2)原子总数相等、价电子总数相等的微粒互为等电子体;
(3)SO3的三聚体中S原子形成4个δ键,以此判断空间构型和杂化类型;SO3的三聚体中每个S形成,存在S=O键和S-O键,S=O键长较短;
(4)Na2O晶胞中阴离子位于晶胞的定点和面心,阳离子位于晶胞的体心,根据晶胞的结构判断配位数,Na的个数为8,O的个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,据此计算质量和体积,进而计算密度.
解答 解:(1)硫是16号元素,有6个价电子,价电子排布图为 ,故答案为:
,故答案为: ;
;
(2)原子总数相等、价电子总数相等的微粒互为等电子体,与SCN-互为等电子体的分子有N2O和CO2,故答案为:N2O和CO2;
(3)SO3的三聚体中S原子形成4个δ键,为sp3杂化;SO3的三聚体中每个S形成,存在S=O键和S-O键,S=O键长较短,即a较短,该分子中含有σ键数目为3×4=12,
故答案为:sp3;a;12;
(4)晶胞中O位于顶点,Na位于体心,每个晶胞中有1个Na与O的距离最近,每个定点为8个晶胞共有,则晶胞中O原子的配位数为8,Na的个数为8,O的个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞的质量为$\frac{4×62g/mol}{6.02×10{\;}^{23}/mol}$,晶胞的体积为(0.566×10-7)3cm3,则晶体F的密度为$\frac{4×62g/mol}{(0.566×10{\;}^{-7}cm){\;}^{3}×6.02×10{\;}^{23}/mol}$=2.27g•cm-3,
故答案为:8;2.27.
点评 本题考查物质结构和性质,侧重考查学生空间想象能力、知识运用能力,涉及晶胞计算、原子结构等知识点,综合性较强,采用均摊法、价层电子对互斥理论等理论分析解答,题目难度中等.

 备战中考寒假系列答案
备战中考寒假系列答案| 编号 | 实验内容 | 实验目的 |
| A | 用平行光照射 | 区别淀粉溶液和氯化钠溶液 |
| B | 加入CaCO3粉末,充分反应后过滤 | 除去CaCl2溶液中的FeCl3 |
| C | 通过灼烧的Cu粉末,收集气体 | 除去N2中的少量O2 |
| D | 滴入稀盐酸,同时用pH计测定至溶液呈中性 | 除去KNO3溶液中的KOH |
[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
淡蓝色 黄绿色.
| A. | 加蒸馏水 | B. | 加浓盐酸 | C. | 加AgNO3溶液 | D. | 加氢氧化钠溶液 |
| A. | 氧化物 | B. | 酸 | C. | 碱 | D. | 盐 |
| A. | 钠 | B. | 氧化钙 | C. | 食盐 | D. | 石灰水 |
 .
.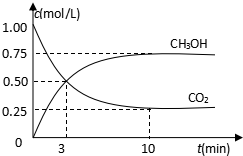 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在485℃时,在体积为1L的密闭容器中,充入1ol CO2和3mol H2,一定条件下发生反应合成甲醇:
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在485℃时,在体积为1L的密闭容器中,充入1ol CO2和3mol H2,一定条件下发生反应合成甲醇: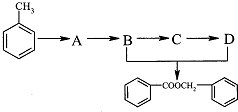
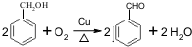
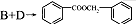 的化学方程式为
的化学方程式为