题目内容
12.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 1L 0.1mol•L-1FeCl3溶液中含有的Fe3+离子数目为0.1NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA | |
| D. | 常温下,2.24LCl2完全与NaOH溶液反应,转移的电子数目一定为0.1NA |
分析 A、铁离子为弱碱阳离子,在溶液中会水解;
B、NaOH对水的电离有抑制作用;
C、反应5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O转移15mol电子,生成4mol氮气;
D、氯气所处状态的压强不明确.
解答 解:A、铁离子为弱碱阳离子,在溶液中会水解,故溶液中的铁离子小于0.1NA个,故A错误;
B、NaOH对水的电离有抑制作用,故溶液中氢氧根几乎全部来自于氢氧化钠的电离,而氢离子全部来自于水的电离,故溶液中水电离出的氢离子和氢氧根的个数为10-13NA个,故B错误;
C、反应5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O转移15mol电子,生成4mol氮气,故当生成28g氮气即1mol氮气时,转移3.75NA个电子,故C正确;
D、氯气所处状态的压强不明确,故气体摩尔体积不明确,氯气的物质的量无法计算,则转移的电子数目无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案
相关题目
13.下列各组金属混合物的质量相同,它们分别与足量盐酸反应,在相同状况下产生的氢气体积也相同,则其中含铝的质量最少的是( )
| A. | 铁和铝 | B. | 锌和铝 | C. | 镁和铝 | D. | 铜和铝 |
3.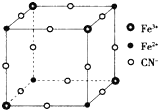 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
 有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )
有一种蓝色晶体[可表示为:MFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上.其晶体中阴离子的最小结构单元如图所示.下列说法错误的是( )| A. | 该晶体的化学式为MFe2(CN)6 | |
| B. | 该晶体熔融可导电,且属于化学变化 | |
| C. | 该晶体属于离子晶体,M呈+2价 | |
| D. | 晶体中与每个Fe3+距离最近且等距离的CN-为6个 |
20.我国科学家在世界上首次合成三种新核素,其中一种新核素的名称是铪-185,关于铪-185,下列说法中正确的是( )
①是一种新元素 ②是一种新原子 ③原子核内有185个质子 ④是铪-180的一种新的核素.
①是一种新元素 ②是一种新原子 ③原子核内有185个质子 ④是铪-180的一种新的核素.
| A. | ①和③ | B. | ②和④ | C. | ②和③ | D. | ③和④ |
7.下列除去杂质的方法正确的是( )
| A. | 除去乙烷中少量的乙烯:通过酸性KMnO4溶液进行分离 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和氢氧化钠溶液洗涤、分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的HCl气体:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
4.下列关于物质分类的说法正确的是( )
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②氯水、次氯酸都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰水混合物、四氧化三铁都不是混合物
⑤电解熔融的Al2O3、12C 转化为14C 都属于化学变化
⑥葡萄糖、油脂都不属于有机高分子.
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②氯水、次氯酸都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰水混合物、四氧化三铁都不是混合物
⑤电解熔融的Al2O3、12C 转化为14C 都属于化学变化
⑥葡萄糖、油脂都不属于有机高分子.
| A. | ①② | B. | ②④ | C. | ③⑤ | D. | ④⑥ |
1.有关下列能量转化的认识不正确的是( )
| A. | 植物的光合作用使得太阳能转化为了化学能 | |
| B. | 燃料燃烧时只是将化学能转化为了热能 | |
| C. | 生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理、有效 | |
| D. | 人类使用照明设备是将电能转化为了光能 |