题目内容
13.同温度下的四种溶液,当NH4+浓度相同时,溶液的物质的量浓度最大的是( )| A. | NH4Al(SO4)2 | B. | NH4Cl | C. | NH3•H2O | D. | CH3COONH4 |
分析 根据铵根离子的浓度和水解的影响角度来分析,如果含有对铵根离子水解起促进作用的离子,则铵根离子水解程度增大,如果含有抑制铵根离子水解的离子,则铵根的水解程度减弱,据此进行判断.
解答 解:物质的量浓度相同的下列溶液中不考虑(水解)其他因素影响,ABD选项中铵根离子浓度分别比为1:1:1,C中NH3•H2O部分电离,铵根离子浓度最小,
A.NH4Al(SO4)2中的铝离子的水解对铵根的水解起抑制作用,导致铵根离子水解程度减小,铵根离子浓度较大;
B.氯化铵中,铵根离子的水解不受氯离子的影响;
C.NH3•H2O是弱电解质,部分电离,其铵根离子浓度最小;
D.醋酸根离子对铵根离子的水解起到促进作用,导致铵根离子水解程度大,溶液中铵根离子浓度较小;
根据分析可知,NH4+的浓度相同时,溶质的浓度最大的是NH3•H2O,
故选C.
点评 本题考查盐的水解原理及其影响、弱电解质的电离,题目难度中等,明确盐的水解原理及其影响因素为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列各对物质中,互为同系物的是( )
| A. | CH3-CH=CH2与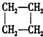 | B. |  与 与 | ||
| C. | 甲苯和二甲苯 | D. | CH2═CH-CH═CH2和CH-CH2-CH2-C≡CH |
18.下列关于1mol甲烷的说法中错误的是( )
| A. | 含有5mol电子 | B. | 含有10mol电子 | ||
| C. | 含有5mol中子 | D. | 含有4mol共用电子对 |
2.NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下2.24L氯气与水充分反应转移电子数为0.1NA | |
| B. | 标况下,2.24LNO2分子总数小于0.1NA | |
| C. | 标准状况下2.24L的CCl4中含有的C-Cl键数为0.4NA | |
| D. | 6.8g液态KHSO4中含有0.1NA个阳离子 |



 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示,2min后反应达到平衡.由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示,2min后反应达到平衡.由图中数据分析: