题目内容
电镀废水有毒成分很多,其中主要有毒性很大的含铬(C+6r)废水与含氰(CN-)废水.
(1)含铬废水中存在如下平衡2CrO42-+2H+?Cr2O72-+H2O,该废水处理工艺中往往先加以酸化,使得(C+6r)在溶液中的主要存在形式是 ;酸化后的溶液加入硫酸亚铁,使(C+6r)转化为毒性较低的Cr3+,写出该反应的离子反应方程式 .
(2)含氰废水在酸性条件下用强氧化剂(NaClO)处理称为“破氰”,破氰后的产物均无毒,该氧化还原反应中的还原产物最可能是 ;氧化产物最可能是 .
(1)含铬废水中存在如下平衡2CrO42-+2H+?Cr2O72-+H2O,该废水处理工艺中往往先加以酸化,使得(C+6r)在溶液中的主要存在形式是
(2)含氰废水在酸性条件下用强氧化剂(NaClO)处理称为“破氰”,破氰后的产物均无毒,该氧化还原反应中的还原产物最可能是
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)根据平衡移动来分析,酸化平衡向正反应方向移动,所以使得(Cr6+)在溶液中的主要存在形式是Cr2O72-,Cr2O72-有强氧化性,亚铁离子有还原性,亚铁离子能被氧化生成铁离子,同时Cr2O72-被还原生成铬离子,根据氧化还原反应中得失电子数相等及原子守恒配平方程式,据此写出离子反应方程式;
(2)根据题意可知,酸性条件下CN-被NaClO反应生成产物均无毒,则根据原子守恒,应该为N2、H2O、CO2和NaCl,根据氧化剂生成还原产物,还原剂生成氧化产物判断;
(2)根据题意可知,酸性条件下CN-被NaClO反应生成产物均无毒,则根据原子守恒,应该为N2、H2O、CO2和NaCl,根据氧化剂生成还原产物,还原剂生成氧化产物判断;
解答:
解:(1)酸化平衡向正反应方向移动,所以使得(Cr6+)在溶液中的主要存在形式是Cr2O72-;Cr元素由Cr2O72-中+6价降低为Cr3+中+3价,共降低6价,Fe元素化合价由Fe2+中+2价升高为Fe3+中+3价,共升高1价,化合价最小公倍数为6,故Cr2O72-系数为1,Fe2+的系数为6,由原子守恒可知,Cr3+的系数为2,Fe3+的系数为6,根据电荷守恒可知,H+为反应物,系数为14,由H元素守恒,H2O为生成物,系数为7,配平后方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,故答案为:Cr2O72-;Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(2)根据题意可知,酸性条件下CN-被NaClO反应生成产物均无毒,则根据原子守恒,应该为N2、H2O、CO2和NaCl,又氧化剂生成还原产物,所以还原产物为NaCl,还原剂生成氧化产物,所以氧化产物为N2、CO2;
故答案为:NaCl;N2、CO2;
(2)根据题意可知,酸性条件下CN-被NaClO反应生成产物均无毒,则根据原子守恒,应该为N2、H2O、CO2和NaCl,又氧化剂生成还原产物,所以还原产物为NaCl,还原剂生成氧化产物,所以氧化产物为N2、CO2;
故答案为:NaCl;N2、CO2;
点评:本题主要考查氧化还原反应基本概念、配平、离子方程式书写等,难度中等,抓住氧化还原反应中基本概念的判断是解题的关键.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、反应SiO2(s)+3C(s)=SiC(s)+2CO(g)室温下不能自发进行,则该反应的△H<0 |
| B、配制硫酸亚铁溶液时,需将FeSO4?7H2O先溶于硝酸再用蒸馏水稀释,最后加少量铁粉 |
| C、0.1 mol?L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 |
| D、在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
对于常温下pH为2的盐酸,下列叙述正确的是( )
| A、c(H+)=c(Cl-)+c(OH-)+c(HCl) |
| B、与等体积pH=12的氨水混合后所得溶液显酸性 |
| C、由H2O电离出的c(H+)=1.0×10-12mol?L-1 |
| D、与等体积0.01mol?L-1乙酸钠溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |
下列有关化学用语表示正确的是( )
A、CO2分子比例模型: |
B、HCl的电子式为: |
| C、乙酸乙酯和葡萄糖的实验式:CH2O |
D、对硝基甲苯的结构简式: |
某反应可用下式表示:mM+4H++O2=mM2++2H2O,根据守恒原理可确定m值为( )
| A、2 | B、3 | C、4 | D、5 |
有如图下4种碳架的烃,则下列判断正确的是( )
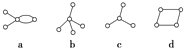

| A、a和d是同分异构体 |
| B、b和c不是同系物 |
| C、a和d都能发生加成反应 |
| D、只有b和c能发生取代反应 |