题目内容
下列叙述正确的是( )
| A、pH相等的盐酸和醋酸溶液中分别加入足量相同的Zn片,反应过程中生成氢气的速率始终相同 | ||
B、室温下向10mL pH=3的醋酸溶液中加水稀释后,溶液中
| ||
| C、醋酸钠溶液中存在反应:CH3COONa+H2O=CH3COOH+NaOH | ||
D、在25℃时,将amol/L的氨水与0.01 mol/L的盐酸等体积混合,充分反应后溶液中c(NH4+)=c(Cl-),则25℃时NH3?H2O的电离常数Kb=
|
考点:弱电解质在水溶液中的电离平衡,盐类水解的原理
专题:
分析:A、反应速率与离子浓度成正比;
B、加水稀释促进电离平衡正向进行,但K不变;
C、醋酸钠溶液的水解应该是可逆符号;
D、在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.01mol/L,根据物料守恒得n(NH3.H2O)=(a-0.01)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3?H2O的电离常数Kb=
.
B、加水稀释促进电离平衡正向进行,但K不变;
C、醋酸钠溶液的水解应该是可逆符号;
D、在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.01mol/L,根据物料守恒得n(NH3.H2O)=(a-0.01)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3?H2O的电离常数Kb=
| c(OH -).c(NH4 +) |
| c(NH 3.H 2O) |
解答:
解:A、反应速率与离子浓度成正比,开始时氢离子浓度相等,所以反应速率相等,但由于CH3COOH是弱电解质,在反应的过程中还要电离出氢离子,所以后来醋酸中氢离子浓度一直大,速率也大,故A错误;
B、CH3COOH?CH3COO-+H+;加水稀释促进电离平衡正向进行,根据K=
=
不变,所以
也不变,故B错误;
C、醋酸钠溶液的水解应该是可逆符号,故C错误;
D、在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.01mol/L,根据物料守恒得n(NH3.H2O)=(a-0.01)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3?H2O的电离常数Kb=
=
=
,故D正确;
故选D.
B、CH3COOH?CH3COO-+H+;加水稀释促进电离平衡正向进行,根据K=
| C(CH 3COO -)C(H +) |
| C(CH 3COOH) |
| C(CH 3COO -)Kw |
| C(CH 3C00H)C(OH -) |
| C(CH3COO -) |
| C(CH3COOH)C(OH -) |
C、醋酸钠溶液的水解应该是可逆符号,故C错误;
D、在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.01mol/L,根据物料守恒得n(NH3.H2O)=(a-0.01)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3?H2O的电离常数Kb=
| c(OH -).c(NH4 +) |
| c(NH 3.H 2O) |
| 10 -7×0.01 |
| a-0.01 |
| 10 -9 |
| a-0.01 |
故选D.
点评:本题主要考查了反应速率的比较、弱电解质的电离、盐类的水解以及计算等,难度不大,掌握原理即可解答.

练习册系列答案
相关题目
某无色混合气体可能含有CO2、CO、H2O(g)、H2中的一种或几种,依次进行如下处理(假设每次处理均反应完全):①通过碱石灰,气体体积减小;②通过灼热的氧化铜时,固体变为红色;③通过无水CuSO4粉末时,粉末变为蓝色;④通过澄清石灰水时,溶液变为浑浊.由此可以确定混合气体中( )
| A、一定含有CO2、H2O蒸气,可能含有H2、CO |
| B、一定含有H2O蒸气、CO,可能含有CO2、H2 |
| C、一定含有CO2、CO,可能含有H2O蒸气、H2 |
| D、一定含有CO、H2,可能含有H2O蒸气、CO2中的1种或2种 |
下列物质属于电解质的是( )
| A、NaCl溶液 | B、油脂 |
| C、NaClO | D、Cu |
实验室中配制250mL 0.5mo1?L-1盐酸时,不需要用到的仪器是( )
| A、酒精灯 | B、玻璃棒 |
| C、容量瓶 | D、胶头滴管 |
下列各化合物的命名正确的是( )
| A、CH2=CH-CH=CH2 1,3-二丁烯 |
B、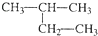 2-甲基丁烷 2-甲基丁烷 |
C、 苯酚 苯酚 |
D、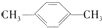 间二甲苯 间二甲苯 |
 如图为实验室某浓硫酸试剂瓶上的标签,回答有关问题:
如图为实验室某浓硫酸试剂瓶上的标签,回答有关问题: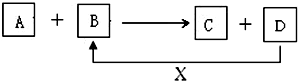 A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)
A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)