题目内容
17.NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 在1 L 0.2 mol•L-1的Na2CO3溶液中含有CO32-的数目为0.2NA | |
| B. | 0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3 NA | |
| C. | 标准状况下22.4 L CH4和C2H4的混合气体所含氢原子数为4NA | |
| D. | 理论上氢氧燃料电池正极消耗11.2 L标准状况下气体时,外线路通过电子数为NA |
分析 A.碳酸根离子为弱酸根离子,水溶液中部分水解;
B.铁参加反应可能生成二价铁离子也能生成三价铁离子;
C.标况下,CH4和C2H4都是气体,1个分子中都含有4个H;
D.依据氢氧燃料电池的原电池原理结合电极反应计算电子转移数;
解答 解:A.碳酸根离子为弱酸根离子,水溶液中部分水解,所以在1 L 0.2 mol•L-1的Na2CO3溶液中含有CO32-的数目小于0.2NA,故A错误;
B.铁参加反应可能生成二价铁离子也能生成三价铁离子,如1mol铁与盐酸反应生成0.1mol二价铁离子,转移的电子数目一定是0.2NA,故B错误;
C.标准状况下22.4 L CH4和C2H4的混合气体所含氢原子数为$\frac{22.4L}{22.4L/mol}$×4×NA=4NA,故C正确;
D.电池中电子守恒,氢氧燃料电池的正极反应为O2+2H2O+4e-=4OH-,消耗11.2L标准状况下气体是0.5molO2,电子转移为2mol,外线路通过电子数为2NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,水溶液中的离子判断,原电池的电极反应与电子转移计算,注意铁发生氧化还原反应价态变化.

练习册系列答案
相关题目
16.已知NO2能被水吸收,反应为3NO2+H2O═2HNO3+NO,在NO2被水吸收的反应中,发生还原反应和氧化反应的物质的质量比为( )
| A. | 3:1 | B. | 1:3 | C. | 1:2 | D. | 2:1 |
17.W、X、Y、Z 是四种短周期非金属元素,原子序数依次增大,X、Y原子核外L电子层的电子数之比为3:4,且Y的原子半径大于X的原子半径,X、Y、Z的最外层电子数之和为16,W的简单离子W-能与水反应生成单质w2.下列说法正确的是( )
| A. | 单质的沸点:X>Z | B. | X与W形成的化合物中只有极性键 | ||
| C. | 阴离子的还原性:W>X | D. | W、X、Y 可形成三元离子化合物 |
5.已知Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,则下列叙述不正确的是( )
| A. | 该反应中旧化学键断裂需要吸收能量,新化学键形成需要放出能量,所以反应前后物质具有的总能量不变 | |
| B. | 上述热化学方程式中的△H的值与实验测定中反应物的用量无关 | |
| C. | 该反应的化学能可以转化为其他形式的能 | |
| D. | 反应物的总能量高于生成物的总能量 |
12.在水中加入等物质的量的Na+、Ag+、Pb2+和SO42-、Cl-、NO3-,然后放入惰性材料做电极的电解槽中,通电片刻,则氧化产物与还原产物的质量比为 ( )
| A. | 35.5:108 | B. | 16:207 | C. | 8:1 | D. | 108:35.5 |
2.某物质在一定条件下按下式分解:2A$\frac{\underline{\;\;△\;\;}}{\;}$B↑+2C↑+D↑测得生成的混合气体质量在相同条件下是同体积H2的15倍,则A的摩尔质量为( )
| A. | 60g•mol-1 | B. | 15g•mol-1 | C. | 30g•mol-1 | D. | 120g•mol-1 |
9.下列各组离子,在水溶液中能大量共存的是( )
| A. | Fe3+、OH- | B. | Na+、SO42- | C. | Ag+、Cl- | D. | H+、OH- |
6.下列化学实验事实及解释都正确的是( )
| A. | 向Na2SO3溶液中加入硝酸酸化的Ba(NO3)2溶液,有白色沉淀出现,说明Na2SO3溶液已经变质 | |
| B. | 某溶液中加入盐酸产生无色气体,该气体能使澄清石灰水变浑浊,说明该溶液中一定有CO32- | |
| C. | 某溶液中加入BaCl2溶液,产生白色沉淀,加稀硝酸后,白色沉淀不溶解,也无其他现象,说明该溶液中一定含有SO42- | |
| D. | 取少量久置的Na2SO3样品溶于水,加足量盐酸有气体产生,然后加BaCl2溶液,产生白色沉淀,说明Na2SO3样品已部分变质 |
7.下列说法正确的是( )
| A. | 按系统命名法,有机物  可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 1 mol  最多能与含3 mol NaOH的水溶液完全反应 最多能与含3 mol NaOH的水溶液完全反应 | |
| C. | 纤维素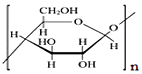 和壳聚糖 和壳聚糖 均属于多糖 均属于多糖 | |
| D. | 在一定条件下,1 mol的  最多能与含3 mol NaOH的溶液完全反应 最多能与含3 mol NaOH的溶液完全反应 |