题目内容
某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示.电池的总反应方程式为2Al+3ClO-+2OH-═3Cl-+2AlO2-+H2O.下列说法正确的是( )

| A、电池的负极反应式为:ClO-+H2O+2e-═Cl-+2OH- |
| B、当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个 |
| C、往滤纸上滴加酚酞试液,b极附近颜色变红 |
| D、b极附近会生成蓝色固体 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据题目信息易拉罐作原电池的负极,失去电子发生氧化反应,石墨电极作正极,C10-在正极上得到电子;外电路中电子从负极流向正极;有1个 mol Al完全溶解时,流经外电路的电子个数为3个,Cu与Al相连为阴极,石墨a为阳极.
解答:
解:A.石墨电极作正极,C10-得到电子,正极反应式为:3C10-+3H20+6e-═3Cl-+60H-,故A错误;
B.当有0.1 mol Al完全溶解时,流经外电路的电子个数约为1.806×1023,电子不能流经电解液,故B错误;
C.b与Al相连为阴极,阴极上氢离子放电,同时生成氢氧根离子,则阴极负极显碱性,酚酞变红色,故C正确;
D.b与Al相连为阴极,阴极上氢离子放电,电极Cu不参与反应,所以b极附近不会生成蓝色固体,故D错误;
故选:C.
B.当有0.1 mol Al完全溶解时,流经外电路的电子个数约为1.806×1023,电子不能流经电解液,故B错误;
C.b与Al相连为阴极,阴极上氢离子放电,同时生成氢氧根离子,则阴极负极显碱性,酚酞变红色,故C正确;
D.b与Al相连为阴极,阴极上氢离子放电,电极Cu不参与反应,所以b极附近不会生成蓝色固体,故D错误;
故选:C.
点评:本题考查了原电池原理和电解池原理的应用,注意电极方程式的书写及利用化合价分析转移电子,题目难度中等.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | ||
B、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-═2AlO
| ||
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | ||
| D、FeCl2溶液中通入足量的Cl2:Fe2++Cl2═Fe3++2Cl- |
下列说法中,不正确的是( )
| A、相对分子质量相同,组成元素的百分含量相同的不同有机物一定是同分异构体的关系 |
| B、碳原子数相同、结构不同的烷烃一定是互为同分异构体关系 |
| C、两有机物互为同系物,则它们也是互为同分异构体关系 |
| D、碳原子数≤10的烷烃,其一氯代物没有同分异构体的烷烃有4种 |
目前市场上的手提应急灯,主要用的是“无液干粉”铅酸蓄电池,其原理是将强腐蚀性的浓硫酸灌注到硅胶中,使电解质溶液不易发生泄漏,大大改善了电池的性能.所用的原料仍然是Pb-PbO2-H2SO4,下列关于该铅酸蓄电池的说法正确的是( )
| A、充电时,电源的正极接蓄电池标“+”的一极,电池上标有“-”的一极发生氧化反应 |
| B、“无液干粉”铅酸蓄电池彻底改变了原来的铅酸蓄电池的原理 |
| C、放电时,在铅酸蓄电池的负极发生还原反应 |
| D、若用此铅酸蓄电池电解饱和NaCl溶液,标准状况下制备1.12LCl2,电池内至少消耗H2SO40.10 mol |
下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
A、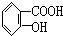 |
B、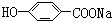 |
| C、H2NCH2COONa |
| D、Na2CO3 |
分析下列各物质的物理性质,可判断其固态不属于分子晶体的是( )
| A、碳化铝,黄色晶体,熔点2200℃.熔融态不导电 |
| B、溴化铝,无色晶体,熔点98℃,熔融态不导电 |
| C、五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、氯仿、丙铜中 |
| D、干冰,无色晶体,熔融时不导电 |
下列有关反应类型说法中正确的是( )
A、由乙二醇制取高分子 是通过加聚反应完成的 是通过加聚反应完成的 |
| B、乙醇在浓硫酸作催化剂,并且加热的条件下一定发生消去反应 |
| C、卤代烃一般来说在NaOH的水溶液中能发生取代反应,而在NaOH的醇溶液中不一定能发生消去反应 |
| D、酯类物质在一定条件下水解一定得到相应的羧酸和醇 |
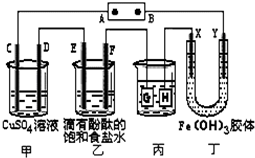 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.