题目内容
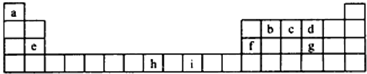
①②③④⑤五种元素,在元素周期表中的位置如图所示.回答下列问题:

(1)①②③④⑤五种元素中,金属性最强的元素是 ,该元素的单质在空气中燃烧的化学方程式为 .
(2)元素①和③可以形成众多的化合物,其中最简单的是(写化学式) 该化合物中,化学键的类型为 (填“离子键”或“共价键”)
(3)画出元素④的原子结构示意图 ,该元素的最高氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)
(4)元素⑤单质在常温下为黄绿色的气体,实验中可以用NaOH溶液吸收,反应的离子方程式为 .

(1)①②③④⑤五种元素中,金属性最强的元素是
(2)元素①和③可以形成众多的化合物,其中最简单的是(写化学式)
(3)画出元素④的原子结构示意图
(4)元素⑤单质在常温下为黄绿色的气体,实验中可以用NaOH溶液吸收,反应的离子方程式为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知①为H、②为Na、③为C、④为N、⑤为Cl.
(1)上述元素中Na的金属性最强,在空气中燃烧生成过氧化钠;
(2)元素①和③可以形成众多的化合物中最简单为甲烷,属于共价化合物,含有共价键;
(3)N原子核外有7个电子,有2个电子层,各层电子数为2、7;Cu与稀硝酸反应生成硝酸铜与NO,与浓硝酸反应生成二氧化氮,反应中氧化剂为硝酸;
(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水.
(1)上述元素中Na的金属性最强,在空气中燃烧生成过氧化钠;
(2)元素①和③可以形成众多的化合物中最简单为甲烷,属于共价化合物,含有共价键;
(3)N原子核外有7个电子,有2个电子层,各层电子数为2、7;Cu与稀硝酸反应生成硝酸铜与NO,与浓硝酸反应生成二氧化氮,反应中氧化剂为硝酸;
(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水.
解答:
解:由元素在周期表中位置,可知①为H、②为Na、③为C、④为N、⑤为Cl.
(1)上述元素中Na的金属性最强,在空气中燃烧生成过氧化钠,反应方程式为:2Na+O2
Na2O2,故答案为:Na;Na2O2;
(2)元素①和③可以形成众多的化合物中最简单为CH4,属于共价化合物,含有共价键,故答案为:CH4;共价键;
(3)N原子核外有7个电子,有2个电子层,各层电子数为2、7,原子结构示意图为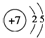 ;Cu与稀硝酸反应生成硝酸铜与NO,与浓硝酸反应生成二氧化氮,反应中氮元素化合价降低,氧化剂为硝酸,故答案为:
;Cu与稀硝酸反应生成硝酸铜与NO,与浓硝酸反应生成二氧化氮,反应中氮元素化合价降低,氧化剂为硝酸,故答案为: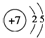 ;HNO3;
;HNO3;
(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
(1)上述元素中Na的金属性最强,在空气中燃烧生成过氧化钠,反应方程式为:2Na+O2
| ||
(2)元素①和③可以形成众多的化合物中最简单为CH4,属于共价化合物,含有共价键,故答案为:CH4;共价键;
(3)N原子核外有7个电子,有2个电子层,各层电子数为2、7,原子结构示意图为
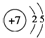 ;Cu与稀硝酸反应生成硝酸铜与NO,与浓硝酸反应生成二氧化氮,反应中氮元素化合价降低,氧化剂为硝酸,故答案为:
;Cu与稀硝酸反应生成硝酸铜与NO,与浓硝酸反应生成二氧化氮,反应中氮元素化合价降低,氧化剂为硝酸,故答案为: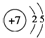 ;HNO3;
;HNO3;(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评:本题考查元素周期表与元素周期律综合应用,难度不大,侧重对基础知识的巩固.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列实验操作中错误的是( )
| A、在由氢氧化铜分解制氧化铜时,要边加热边用玻璃棒搅拌 |
| B、用药匙或者纸槽把粉末状药品送入试管的底部 |
| C、过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
| D、刚完成蒸发结晶,因要做下一个实验,可以将蒸发皿先放在桌面上,冷却后收好 |
已知反应H2(g)+Cl2(g)=2HCl(g)△H=-184.6kJ?mol-1,则反应HCl(g)=
H2(g)+
Cl2(g)的△H为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、+184.6 kJ?mol-1 |
| B、-92.3 kJ?mol-1 |
| C、-369.2 kJ?mol-1 |
| D、+92.3 kJ?mol-1 |
 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图:
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如图: