题目内容
7.设NA为阿伏加德罗常数的值.下列叙述正确的是( )| A. | 0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA | |
| B. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA | |
| C. | 常温常压下,14 g C2H4和C3H6的混合气体中含有碳原子的数目为NA | |
| D. | 25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
分析 A、氯气和水的反应为可逆反应;
B、求出丙烷的物质的量,然后根据丙烷中含10对共用电子对来分析;
C、C2H4和C3H6的最简式均为CH2;
D、pH=12的Na2CO3溶液中钠离子的浓度无法计算.
解答 解:A、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子数小于0.1NA个,故A错误;
B、标况下0.56L丙烷的物质的量为0.025mol,而丙烷中含10对共用电子对,故0.025mol丙烷中含0.25NA条共价键,故B错误;
C、C2H4和C3H6的最简式均为CH2,故14g混合物中含有CH2的物质的量为1mol,故含NA个碳原子,故C正确;
D、pH=12的Na2CO3溶液中钠离子的浓度无法计算,故溶液中的钠离子的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
2.某些儿童由于偏食(不爱吃蔬菜、水果),结果生长发育出现障碍,患营养缺乏症.这是由于下列哪种物质不足而引起的( )
| A. | 维生素 | B. | 油脂 | C. | 蛋白质 | D. | 糖类 |
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 7.8gNa2O2固体中含离子总数为0.4NA | |
| B. | 2.0gH218O和D216O的混合物中所含中子数为NA | |
| C. | 常温下,22.4LCH4中含C-H共价键数为4NA | |
| D. | 标准状况下,3.36 L氟化氢中含有的电子数目为1.5NA |
15.在汽车尾气处理装置中加入适当的催化剂,能发生反应:4CO+2NO2=4CO2+N2.下列有关该反应的说法正确的是( )
| A. | CO发生氧化反应 | B. | NO2是还原剂 | C. | CO是氧化剂 | D. | N元素化合价升高 |
2.如图所示的实验操作与方法正确的是( )
| A. | 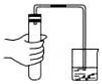 检验装置气密性 | B. | 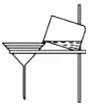 过滤 | C. |  点燃酒精灯 | D. | 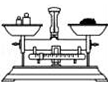 称量氯化钠 |
12.根据下列物质中N元素的化合价判断,其中说法错误的是( )
| A. | NH3具有还原性 | B. | N2只具有还原性 | C. | N2只具有氧化性 | D. | HNO3具有氧化性 |
19.下列说法中正确的是(NA代表阿伏加德罗常数的值)( )
| A. | 28 g N2和28 g CO所含的分子数都是NA | |
| B. | 2 g H2和2g O2所含的原子数都是NA | |
| C. | 28 g CO和44 g CO2所含的氧原子数都是2NA | |
| D. | 98 g H2SO4和98 g H3PO4所含的氧分子数都是4NA |
16.Fe(OH)3胶体和MgCl2溶液共同具备的性质是( )
| A. | 加热时,二者均能稳定存在 | B. | 两者均有丁达尔效应 | ||
| C. | 加入盐酸先沉淀,后溶解 | D. | 分散质微粒可通过滤纸 |
17.(1)表给出几种物质的熔点,对此有下列一些说法:
①CaCl2属于离子晶体 ②SiCl4是分子晶体
③一个SiO2分子由1个Si原子和2个O原子构成 ④MgCl2在熔化状态不能导电 上述说法中正确的有①②
(2)1g氢气燃烧生成液态水时,放出142.9kJ的热量,写出热化学方程式H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol
(3)已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)═CO2(g)△H=-393.51 KJ•mol-1
C(金刚石)+O2(g)═CO2(g)△H=-395.41 KJ•mol-1
据此判断,由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低.
①CaCl2属于离子晶体 ②SiCl4是分子晶体
| 物质 | SiO2 | MgCl2 | CaCl2 | SiCl4 |
| 熔点(℃) | 1723 | 712 | 782 | -68 |
(2)1g氢气燃烧生成液态水时,放出142.9kJ的热量,写出热化学方程式H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol
(3)已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)═CO2(g)△H=-393.51 KJ•mol-1
C(金刚石)+O2(g)═CO2(g)△H=-395.41 KJ•mol-1
据此判断,由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低.