题目内容
8.物质的量与摩尔质量的联系:(1)1molH2O的质量是18g,H2O的摩尔质量是18g/mol.
1molMg的质量是24g,Mg的摩尔质量是24g/mol.
Na+的摩尔质量是23g/mol,NO2-的摩尔质量是46g/mol.
2molH2的质量是4g,1molO2的质量是32g.2molH2O的质量是36g.
(2)64gO2的物质的量是2mol.24.5gH2SO4的物质的量是0.25mol.
分析 (1)摩尔质量与相对分子质量的数值相同,结合m=nM计算;
(2)结合n=$\frac{m}{M}$计算.
解答 解:(1)1molH2O的质量是1mol×18g/mol=18g,H2O的摩尔质量是18g/mol,
1molMg的质量是1mol×24g/mol=24g,Mg的摩尔质量是24g/mol,
Na+的摩尔质量是23g/mol,NO2-的摩尔质量是46g/mol,
2molH2的质量是2mol×2g/mol=4g,1molO2的质量是1mol×32g/mol=32g,2molH2O的质量是2mol×18g/mol=36g,
故答案为:18g;18g/mol;24g;24g/mol;23g/mol;46g/mol;4g;32g;36g;
(2)64gO2的物质的量是$\frac{64g}{32g/mol}$=2mol,24.5gH2SO4的物质的量是$\frac{24.5g}{98g/mol}$=0.25mol,
故答案为:2mol;0.25mol.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.在一支50mL滴定管中盛入0.1mol/L HCl溶液,其液面恰好在20mL刻度处.若把滴定管中的溶液全部放入锥形瓶中,然后以0.1mol/L NaOH溶液进行滴定,当恰好中和时,消耗NaOH溶液的体积( )
| A. | 等于20 mL | B. | 等于30 mL | C. | 大于30 mL | D. | 小于20 mL |
16.下列说法正确的是( )
| A. | 还原性:K>Na>Mg | B. | 氢化物的稳定性:H2O<H2S<H2Se | ||
| C. | 酸性:H3PO4<H2SO4<HCl | D. | 原子半径:Na<Mg<Al |
3.有3种溶液①0.01mol•L-1醋酸; ②0.02mol•L-1醋酸与0.02mol•L-1NaOH等体积混合后的溶液;③0.04mol•L-1醋酸与0.02mol•L-1 NaOH等体积混合后的溶液.下列说法不正确的是( )
| A. | 相同温度下,溶液中水的电离程度:溶液①<溶液② | |
| B. | 可用Na2CO3固体鉴别0.04mol•L-1醋酸和0.04mol•L-1盐酸 | |
| C. | 向①中加入少量CH3COONa固体,则$\frac{{K}_{a}}{c(C{H}_{3}CO{O}^{-})}$增大 | |
| D. | 加水稀释溶液③,溶液中$\frac{c(C{H}_{3}COOH)•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$不变 |
1.下列实验操作中.不正确的是( )
| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 用渗析法除去Fe(OH)3胶体中的Cl- | |
| C. | 除去溴乙烷中的乙醇,用水洗后,再用分液漏斗分离 | |
| D. | 用盐析法分离硬脂酸钠和甘油 |
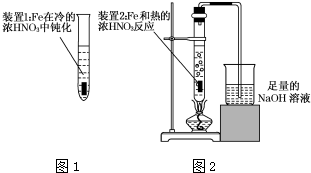 Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题:
Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题: