题目内容
用下列装置进行相应实验,能达到实验目的是( )
A、 用于Cu和浓H2SO4反应制取少量的SO2气体 |
B、 用于制备并收集NH3 |
C、 可形成原电池并获得稳定电流 |
D、 用于检验制得的乙烯中是否混有SO2和CO2 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.Cu和浓H2SO4反应需要加热;
B.氨气采用向下排空气法收集;
C.含有盐桥的原电池中,电极材料和相对应的可溶性电解质溶液含有相同的金属元素;
D.乙烯能被酸性高锰酸钾氧化.
B.氨气采用向下排空气法收集;
C.含有盐桥的原电池中,电极材料和相对应的可溶性电解质溶液含有相同的金属元素;
D.乙烯能被酸性高锰酸钾氧化.
解答:
解:A.Cu和浓H2SO4反应需要加热,图中装置没有加热,则不能发生反应,故A错误;
B.氨气的密度小于空气,且常温下和空气不反应,所以氨气采用向下排空气法收集,故B错误;
C.含有盐桥的原电池中,电极材料和相对应的可溶性电解质溶液含有相同的金属元素,且该反应能自发进行,铜为负极,Pt为正极,所以能形成原电池,故C正确;
D.乙烯被酸性高锰酸钾氧化生成二氧化碳,且SO2被酸性高锰酸钾氧化掉,不能使品红褪色,不能确定是否含有SO2,故D错误.
故选C.
B.氨气的密度小于空气,且常温下和空气不反应,所以氨气采用向下排空气法收集,故B错误;
C.含有盐桥的原电池中,电极材料和相对应的可溶性电解质溶液含有相同的金属元素,且该反应能自发进行,铜为负极,Pt为正极,所以能形成原电池,故C正确;
D.乙烯被酸性高锰酸钾氧化生成二氧化碳,且SO2被酸性高锰酸钾氧化掉,不能使品红褪色,不能确定是否含有SO2,故D错误.
故选C.
点评:本题考查化学实验方案的评价,涉及气体的制取、收集以及原电池等,侧重气体的制备实验考查,题目难度不大.

练习册系列答案
相关题目
 铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+| 放电 |
| 充电 |
| A、氧化性:Cr3+>Fe3+ |
| B、电池放电时,负极的电极反应式为Fe2+-e-═Fe3+ |
| C、充电时,阴极的电极反应式为Cr3++e-═Cr2+ |
| D、电池放电时,Cl-从负极室穿过选择性透过膜移向正极室 |
下列分散系中,分散质粒子直径最大的是( )
| A、雾 | B、石灰乳 |
| C、氢氧化铁胶体 | D、氯化钠溶液 |
下列反应的离子方程式正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | ||||
B、NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-
| ||||
| C、漂白粉溶液中通入足量的SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | ||||
| D、明矾溶液与氢氧化钡溶液反应,使 SO2-恰好完全沉淀:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
盛满等体积NO与NO2的混合气体的100mL量筒,倒置于水槽中,通入多少氧气恰好能使量筒中充满硝酸水溶液( )
| A、100mL |
| B、50mL |
| C、37.5mL |
| D、12.5mL |
下列物质依次按照混合物、氧化物、弱电解质和非电解质的顺序排列的一组是( )
| A、淀粉、CuO、HClO、Cu |
| B、普通玻璃、H2O、Fe(SCN)3、葡萄糖 |
| C、KAl(SO4)2?12H2O、KClO3、NH3?H2O、CH3CH2OH |
| D、水玻璃、Na2O?CaO?6SiO2、Ag2O、SO3 |
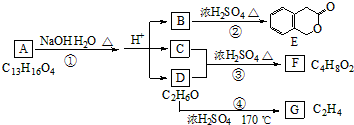
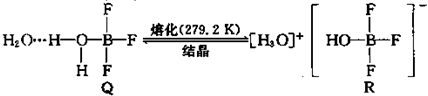
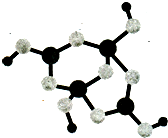 运用物质结构的知识完成B、N元素的问题.
运用物质结构的知识完成B、N元素的问题.