题目内容
(8分)氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。氯碱工业中制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。学校实验小组精制粗盐水的实验过程如下:
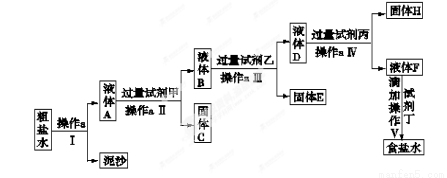
请回答以下问题:
(1)操作a的名称是 ,所用玻璃仪器是 。
(2)在第Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为 溶液。
(3)判断加入试剂乙已过量的方法是 。
(4)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式 。
(1) 过滤 玻璃棒、漏斗、烧杯
(2)NaOH (3)加入试剂乙氯化钡溶液后静置分层后取上层清夜,继续滴加几滴氯化钡溶液后,若无明显现象,则证明加入的试剂乙已过量。(答案合理即可)。(4)NaOH+HCl=NaCl+H2O Na2CO3+HCl=NaCl+H2O+CO2↑
【解析】
试题分析:(1)在食盐水中,实现溶液和泥沙难溶物的分离可以采用过滤的方法,故答案为:过滤;(2)加入过量试剂氢氧化钠后,可以将镁离子以及铁离子形成氢氧化镁和氢氧化铁沉淀;氯化钡可以让硫酸根离子形成硫酸钡沉淀,碳酸钠可以让钙离子以及过量的钡离子形成碳酸钙和碳酸钡沉淀,并且碳酸钠必须加在氯化钡之后,故答案为:NaOH;(3)通过分析乙是氯化钡溶液,判读乙试剂过量的方法是加入乙试剂后,取上层清液,继续滴加几滴氯化钡溶液,若无明显现象,则证明加入的试剂乙已过量。(4)在第Ⅴ步中,加入试剂盐酸可以讲过量的氢氧化钠以及过量的碳酸钠除掉,此过程的化学方程式为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
考点:粗盐提纯。

(8分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1NaOH溶液,实验尚缺少的玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
实验用品 | 溶液温度 | 中和热 | ||||
T1 | t2 | ΔH | ||||
① | 50 mL0.55 mol·L-1 NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.3 ℃ |
| |
② | 50 mL0.55 mol·L-1 NaOH溶液 | 50 mL0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.5 ℃ | ||
(已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。)
根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或 “无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。
 2CO(g);2CO(g) + O2(g)
2CO(g);2CO(g) + O2(g)  2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法,其中正确的是
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法,其中正确的是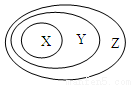

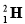 ②H2O、D2O ③
②H2O、D2O ③
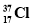 ④金刚石、石墨 ⑤O2、O3 ⑥H2、H+
④金刚石、石墨 ⑤O2、O3 ⑥H2、H+