题目内容
11.下列化学用语对应正确的是( )| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 硫原子的结构示意图: | |
| C. | 基态18O的电子排布式:1s22s22p63s23p6 | |
| D. | CH4分子的比例模型: |
分析 A.乙烯的结构简式中必须标出碳碳双键;
B.硫原子的核电荷数=核外电子总数=16,最外层含有6个电子;
C.基态18O的核外电子总数为8,不是18;
D. 为球棍模型,不是比例模型.
为球棍模型,不是比例模型.
解答 解:A.乙烯分子中含有1个碳碳双键,乙烯正确的结构简式为:CH2=CH2,故A错误;
B.硫原子的核电荷数、核外电子总数都是16,其结构示意图为: ,故B正确;
,故B正确;
C.基态18O的核外电子总数为8,其正确的电子排布式为:1s22s22p4,故C错误;
D.CH4分子为正四面体结构,碳原子相对体积大于氢原子,其正确的比例模型为: ,故D错误;
,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及原子结构示意图、比例模型与球棍模型、结构简式、电子排布式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.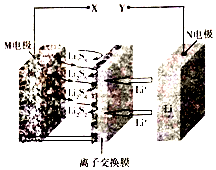 新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )
新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )
 新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )
新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )| A. | 电池充电时X为电源负极 | |
| B. | 放电时,正极上可发生反应:2Li++Li2S4+2e-=2Li2S2 | |
| C. | 充电时,每生成1molS8转移0.2mol电子 | |
| D. | 离子交换膜只能通过阳离子,并防止电子通过 |
2.戊醇(C5H11OH)与下列物质发生反应时,所得产物可能结构种数最少(不考虑立体异构)的是( )
| A. | 与浓硫酸共热消去 | B. | 与浓氢溴酸卤代 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
19.下列各组元素中,属于同一周期的是( )
| A. | H、Na | B. | N、Cl | C. | Mg、Si | D. | O、S |
16.向200mL 0.5mol/L的FeCl3溶液中加入一定体积的0.5mol/L的NaOH溶液,产生5.35g沉淀,则加入的NaOH溶液的体积是( )
| A. | 200 mL | B. | 300 mL | C. | 600 mL | D. | 700 mL |
3.下列物质属于纯净物的是( )
| A. | 漂白粉 | B. | 氯水 | C. | 液氯 | D. | 水玻璃 |
20.下列说法正确的是( )
| A. | 导电性强的溶液一定是强电解质溶液 | |
| B. | H2SO4是强电解质,稀硫酸中没有H2SO4分子 | |
| C. | NaCl晶体是由Na+和Cl-组成,NaCl晶体是良导体 | |
| D. | 氯气和氨气的水溶液导电性都很好,所以它们是强电解质 |
1.反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.下列叙述不正确的是( )
| A. | 氧化剂为KMnO4,其中Cl元素被还原 | |
| B. | 若有0.8molH2O生成,则反应中有NA个电子转移 | |
| C. | 浓HCl在反应中起酸性和还原性的作用 | |
| D. | 由此反应可以大胆推测氧化性强弱关系:KMnO4>MnO2 |
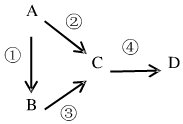 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.