题目内容
现有常见金属A存在如下的转化关系(如图中有些反应的产物和反应的条件没有全部标出),其中E为白色沉淀.
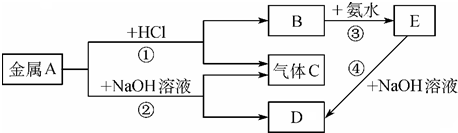
请回答下列问题:
(1)保存金属A不需要特殊的防护措施,其原因是 .
(2)上述4个转化关系中属于氧化还原反应的共有 个.
(3)反应②的化学方程式为 .
(4)反应③的离子方程式为 .

请回答下列问题:
(1)保存金属A不需要特殊的防护措施,其原因是
(2)上述4个转化关系中属于氧化还原反应的共有
(3)反应②的化学方程式为
(4)反应③的离子方程式为
考点:无机物的推断
专题:
分析:金属A能与既能与盐酸反应生成气体C,又能与NaOH反应生成气体C,则A为Al,C为H2,B为AlCl3,D为NaAlO2,E为Al(OH)3,据此解答.
解答:
解:金属A能与既能与盐酸反应生成气体C,又能与NaOH反应生成气体C,则A为Al,C为H2,B为AlCl3,D为NaAlO2,E为Al(OH)3,
(1)金属铝表面易形成致密的氧化物保护膜,能防止被腐蚀,故答案为:金属铝表面易形成致密的氧化物保护膜,能防止被腐蚀;
(2)上述4个转化关系中的反应①2Al+6HCl=AlCl3+3H2↑②2Al+2NaOH+2H2O=2NaAlO2+3H2↑,有2个反应属于氧化还原反应,故答案为:2;
(3)反应②为铝与氢氧化钠反应,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)反应③为氯化铝与氨水反应,反应的离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
(1)金属铝表面易形成致密的氧化物保护膜,能防止被腐蚀,故答案为:金属铝表面易形成致密的氧化物保护膜,能防止被腐蚀;
(2)上述4个转化关系中的反应①2Al+6HCl=AlCl3+3H2↑②2Al+2NaOH+2H2O=2NaAlO2+3H2↑,有2个反应属于氧化还原反应,故答案为:2;
(3)反应②为铝与氢氧化钠反应,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)反应③为氯化铝与氨水反应,反应的离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
点评:本题考查无机物推断,“A能与酸、碱反应生成气体C”是推断的突破口,在结合转化关系推断,难度中等.

练习册系列答案
相关题目
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②少许H2O ③升温 ④CH3COONa固体 ⑤降温 ⑥KCl溶液.
①NaOH固体 ②少许H2O ③升温 ④CH3COONa固体 ⑤降温 ⑥KCl溶液.
| A、②④⑤⑥ | B、①② |
| C、②③⑤ | D、②⑤⑥ |
实验室要用98%的浓硫酸(密度为1.84g?ml-1)配制0.5mol?L-1硫酸溶液480ml,选用的主要仪器有烧杯、胶头滴管、玻璃棒、量筒,还缺少( )
| A、容量瓶 |
| B、250ml容量瓶 |
| C、分液漏斗 |
| D、500ml容量瓶 |
配制一定物质的量浓度的NaOH溶液,下列叙述正确的是( )
| A、称量时,将NaOH固体直接放在托盘天平的左盘上 |
| B、将NaOH固体在烧杯中溶解后立即转移至容量瓶中 |
| C、定容时,俯视容量瓶的刻度线会使所配溶液的浓度偏高 |
| D、定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 30mL盐酸 | 30mL盐酸 | 30mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A、向50 mL盐酸中加入混合物27.6 g时,盐酸过量 |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、15.7 g混合物与盐酸恰好能完全反应 |
| D、盐酸的物质的量浓度为5.0 mol/L |
铁及其合金在生产、生活中应用广泛,下列说法中正确的是( )
| A、生铁中含有碳,抗腐蚀能力比纯铁强 |
| B、铁与盐溶液所发生的反应都是置换反应 |
| C、铁与稀硫酸反应,铁与浓硫酸不能反应 |
| D、工业上可以用铝热反应的方法制取少量的铁 |
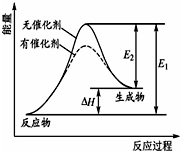 某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂能改变反应的焓变 |
| C、催化剂能降低反应的活化能E1和 E2 |
| D、增大反应物的浓度,可使单位体积内活化分子百分数增大,反应速率加快 |
下列物质中有自由移动的氯离子的是( )
| A、氯化钠晶体 |
| B、熔化的氯化钾 |
| C、氯酸钾溶液 |
| D、液态氯化氢 |
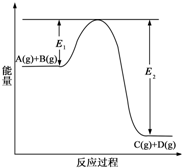 (1)反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
(1)反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.