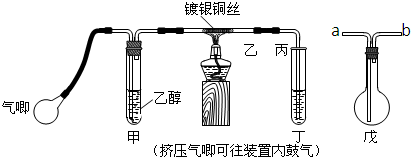
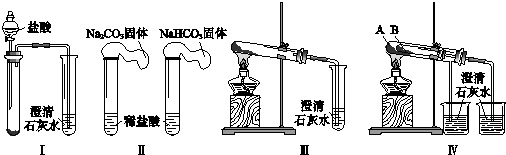
题目内容
1.明矾的水溶液显酸性,可做净水剂的原因是Al3++3H2O?Al(OH)3+3H+(写有关的离子方程式).分析 明矾中铝离子水解生成氢离子和氢氧化铝,溶液显酸性;可做净水街是由于铝离子能水解生成氢氧化铝胶体.
解答 解:明矾溶液中的Al3+属于弱碱阳离子,能水解生成氢离子和氢氧化铝,故溶液显酸性,生成的氢氧化铝胶体具有吸附性,故能净水,其离子方程式为Al3++3H2O?Al(OH)3+3H+;
故答案为:酸;Al3++3H2O?Al(OH)3+3H+.
点评 本题考查盐类水解,明确水解规律即可解答,题目难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
6.下列说法不正确的是( )
| A. | 常温下,pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 | |
| B. | 叠氮酸(HN3)与醋酸酸性相似,NaN3水溶液中离子浓度大小顺序为c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| C. | 常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH4+)=c(Cl-) | |
| D. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
13.液氨与水的电离相似,存在微弱的电离:2NH3+NH3NH4++NH2-.对该体系的说法中错误的是( )
| A. | 液氨中c(NH4+)与c(NH2-)的乘积为一常数 | |
| B. | 液氨电离达到平衡时,各微粒的浓度保持不变 | |
| C. | 只要不加入其它物质c(NH4+)=c(NH2-) | |
| D. | 液氨中存在NH3、NH4+、NH2-、H2O、NH3•H2O等粒子 |
10.下列有关计的方案能达到实验目的是( )
| A. | 制备Fe(OH)3胶体:向0.1mol•L-1FeCl3溶液中加入等体积0.3mol•L-1NaOH溶液 | |
| B. | 除去FeCl3溶液中少量Cu2+:向含有少量Cu2+的FeCl3溶液中加入适量铁粉至蓝色刚好消失后过滤 | |
| C. | 等浓度的碳酸钠溶液和硫酸钠溶液,前者碱性强,可以证明硫的非金属性比碳强 | |
| D. | 验证氧化性Fe3+<Br2<Cl2:向试管中依次加入1mL 0.1mol•L-1FBr2溶液、几滴KSCN 溶液和1mL苯,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,观察整个过程中有机相和水相中的现象 |
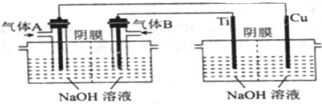 (1)工业上可利用CO2和H2生产甲醇,方程式如下:
(1)工业上可利用CO2和H2生产甲醇,方程式如下: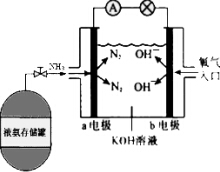 氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.氨氧燃料电池示意图,回答下列问题.
氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.氨氧燃料电池示意图,回答下列问题.