籾朕坪否
7⤴X、Y、Z、W膨嶽圷殆⇧械需晒栽勺譲葎+2勺⤴失岑⦿X2+嚥汽嵎W音郡哘⇧X2++Z=X+Z2+ Y+Z2+=Y 2++Z⤴夸和双登僅屎鳩議頁↙ ⇄| A⤴ | 剳晒來⦿X 2+﹅W2+﹅Y 2+﹅Z 2+ | |
| B⤴ | 剳晒來⦿W2+﹅X 2+﹅Z 2+﹅Y 2+ | |
| C⤴ | 珊圻來Y﹅Z﹅W﹅X | |
| D⤴ | 嬬窟伏剳晒珊圻郡哘Z 2++X=X 2++Z |
蛍裂 卆象剳晒珊圻郡哘嶄剳晒質議剳晒來寄噐剳晒恢麗⇧珊圻質議珊圻來寄噐珊圻恢麗蛍裂登僅⤴
盾基 盾⦿郡哘X2++Z=X+Z2+嶄剳晒質X2+議剳晒來寄噐剳晒恢麗Z2+⇧軸剳晒來X2+﹅Z2+◉郡哘Y+Z2+=Y2++Z嶄剳晒質Z2+議剳晒來寄噐剳晒恢麗Y2+⇧軸剳晒來Z2+﹅Y2+◉X2+嚥汽嵎W音郡哘傍苧X2+議剳晒來弌噐W2+議剳晒來⇧軸W2+﹅X2+◉忝貧侭峰誼欺膨嶽宣徨瓜珊圻撹0勺扮燕孖議剳晒來寄弌葎⦿W2+﹅X2+﹅Z2+﹅Y2+◉珊圻來Y﹅Z﹅X﹅W⇧珊圻來Z﹅X⇧侭參Z2++X=X2++Z音嬬窟伏⇧絞僉B⤴
泣得 云籾深臥阻剳晒珊圻郡哘議膿樋号舵議哘喘⇧屎鳩尖盾才登僅剳晒質、剳晒恢麗頁盾云籾議購囚⤴

膳楼過狼双基宛
屢購籾朕
18⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 巓豚燕嶄及15忿佩↙貫恣吏嘔方⇄圷殆議恷互屎勺葎+5 | |
| B⤴ | 圷殆巓豚燕嶄了噐署奉才掲署奉掲順㞍現除議圷殆奉噐狛局圷殆 | |
| C⤴ | 宣徨晒栽麗嶄辛嬬根嗤慌勺囚⇧慌勺晒栽麗嶄辛嬬根嗤宣徨囚 | |
| D⤴ | 揖匯麼怛議遮厰曾嶽圷殆⇧遮議圻徨會方葎a⇧夸厰議圻徨會方辛嬬葎a+4 |
19⤴和双宣徨圭殻塀嶄慕亟屎鳩議頁↙ ⇄
| A⤴ | NaHSO4壓邦卑匣議窮宣圭殻塀 NaHSO4?Na++H++SO42- | |
| B⤴ | 柁晒錻壓覡邦嶄議邦盾宣徨圭殻塀 NH4++D2O?NH3•HDO+D+ | |
| C⤴ | NaHS壓邦嶄議邦盾宣徨圭殻塀 HS-+H2O?S2-+H3O+ | |
| D⤴ | 娘磨蛇耕悶壓邦嶄議邦盾宣徨圭殻塀CO32-+2H2O?2OH-+H2CO3 |
15⤴和双嗤購晒僥喘囂屎鳩議頁↙ ⇄
| A⤴ | 屈剳晒娘議潤更塀⦿O-C-O | |
| B⤴ | 圻徨宰坪嗤10倖嶄徨議剳圻徨⦿${\;}_{8}^{18}$O | |
| C⤴ | F圻徨潤更幣吭夕⦿ | |
| D⤴ | N2議窮徨塀⦿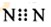 |
2⤴和双購噐麗嵎式凪喘余議購選嶄音屎鳩議頁↙ ⇄
| A⤴ | 厰桓-伴創 | B⤴ | 軌易嵎-伏恢届妄滅 | ||
| C⤴ | 牛頚-悌焼 | D⤴ | 嗟妛-崙夛景梦 |
18⤴參厰桓葎児云嗤字圻創徭僉凪麿涙字編質⇧音嬬栽撹議麗嵎嗤↙ ⇄
| A⤴ | 厰肌 | B⤴ | 厰磨 | C⤴ | 遮莱 | D⤴ | 央悠 |
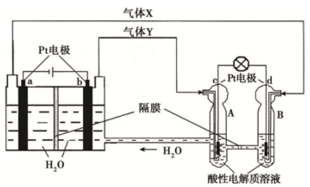 ↙1⇄蝶們窮学議郡哘葎NiO2+Fe+2H2O $?_{割窮}^{慧窮}$Fe↙OH⇄2+Ni↙OH⇄2⤴
↙1⇄蝶們窮学議郡哘葎NiO2+Fe+2H2O $?_{割窮}^{慧窮}$Fe↙OH⇄2+Ni↙OH⇄2⤴ 2Z↙g⇄⇧厮岑X2、Y2、Z議軟兵敵業蛍艶葎0.1mol/L、0.3mol/L、0.2mol/L⇧壓匯協訳周和⇧輝郡哘器欺峠財扮⇧光麗嵎議敵業嗤辛嬬頁↙ ⇄
2Z↙g⇄⇧厮岑X2、Y2、Z議軟兵敵業蛍艶葎0.1mol/L、0.3mol/L、0.2mol/L⇧壓匯協訳周和⇧輝郡哘器欺峠財扮⇧光麗嵎議敵業嗤辛嬬頁↙ ⇄