题目内容
某实验室的尾气中含有较多的氯气,下列试剂用来吸收氯气最适合的是( )
| A、澄清的石灰水 |
| B、饱和食盐水 |
| C、自来水 |
| D、NaOH溶液 |
考点:氯气的化学性质
专题:卤族元素
分析:氯气微溶于水,难溶于饱和食盐水,可与氢氧化钠等溶液发生反应而被吸收,结合吸收尾气的效果来分析解答.
解答:
解:A.澄清的石灰水浓度较小,不能充分吸收氯气,故A不选;
B.食盐水中氯离子浓度较大,抑制氯气的溶解,则吸收效果最不好,故B不选;
C.氯气微溶于水,吸收效果不好,故C不选;
D.因氯气能与烧碱反应,且相同条件下,氢氧化钠的溶解度大于氢氧化钙的溶解度,则烧碱溶液的吸收效果好,故D选.
故选D.
B.食盐水中氯离子浓度较大,抑制氯气的溶解,则吸收效果最不好,故B不选;
C.氯气微溶于水,吸收效果不好,故C不选;
D.因氯气能与烧碱反应,且相同条件下,氢氧化钠的溶解度大于氢氧化钙的溶解度,则烧碱溶液的吸收效果好,故D选.
故选D.
点评:本题考查氯气的尾气处理,为高频考点,明确氯气的化学性质是解答本题的关键,并注意信息中“最合适”的试剂来分析解答.

练习册系列答案
相关题目
下列各面组物质的溶液逐滴互滴,前一种溶液逐滴滴入后一种溶液中,与后一种溶液逐滴滴入前一种溶液中产生的现象相同的是( )
①NaHCO3和HCl ②HNO3和Na[Al(OH)4]③AlCl3 和NaOH ④Ca(HCO3)2和Ca(OH)2
⑤Na2CO3和HCl.
①NaHCO3和HCl ②HNO3和Na[Al(OH)4]③AlCl3 和NaOH ④Ca(HCO3)2和Ca(OH)2
⑤Na2CO3和HCl.
| A、①⑤ | B、②④ | C、②⑤ | D、①④ |
有关常温下pH均为11的氨水和Ba(OH)2溶液的说法正确的是( )
| A、两溶液中,由水电离出的氢氧根离子浓度均为1×10-11mol/L |
| B、分别加水稀释100倍后,两种溶液的pH均变为9 |
| C、氨水中的c(NH+)和Ba(OH)2溶液中的c(Ba2+)相等 |
| D、分别加入等量的pH为1的硫酸,二者的导电能力均减小 |
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一.下列对有关实验事实的解释正确的是( )
| A、SO2使酸性高锰酸钾溶液褪色,体现了SO2的漂白性 |
| B、在含FeCl2、NaBr和KI的混合溶液中滴加少量新制氯水,首先生成的是Fe3+ |
| C、将CO2通入BaCl2溶液中有白色沉淀生成 |
| D、浓硝酸久置变黄,是因为浓硝酸分解生成的有色产物溶于其中的缘故 |
为了净化和收集由盐酸和大理石制得的CO2气体,从下图中选择合适的装置并连接合理的是( )

| A、a-a′→d-d′→e |
| B、b-b′→d-d′→g |
| C、c-c′→d-d′→g |
| D、d-d′→c-c′→f |
能确认化学平衡一定发生移动的是( )
| A、化学反应速率发生了改变 |
| B、可逆反应达到平衡后,使用催化剂 |
| C、有气态物质参加的可逆反应达到平衡后,改变压强 |
| D、由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
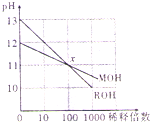 常温下,两种一元碱MOH和ROH的溶液分别加水稀释时,pH变化如图所示.下列有关说法正确的是( )
常温下,两种一元碱MOH和ROH的溶液分别加水稀释时,pH变化如图所示.下列有关说法正确的是( )| A、RCl溶液pH<7 |
| B、稀释前,c(ROH)=10c(MOH) |
| C、在x点,c(M+)=c(R+) |
| D、等体积的pH=12的MOH溶液和pH=2的盐酸混合,c(M+)=c(Cl-) |
 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同.回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同.回答下列问题: