题目内容
16.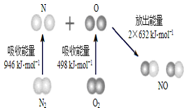 根据如图所示的N2 (g)和O2(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是( )
根据如图所示的N2 (g)和O2(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是( )| A. | N2(g) 与O2(g)反应生成NO(g)是放热反应 | |
| B. | 2 mol O原子结合生成O2(g)时需要吸收498 kJ能量 | |
| C. | 1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量 | |
| D. | 该反应中反应物总能量高于生成物总能量 |
分析 由图可知,断裂化学键吸收能量,成键释放能量,且焓变等于吸收能量减去释放能量,则N2(g)+O2(g)=2NO(g)△H=946kJ/mol+498kJ/mol-2×632kJ/mol=+180kJ/mol,可知反应是吸热反应,以此来解答.
解答 解:A.生成NO的反应为吸热反应,故A错误;
B.2 mol O原子结合生成O2(g)时需要释放498 kJ能量,故B错误;
C.由图可知,1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量,故C正确;
D.为吸热反应,则反应物总能量低于生成物总能量,故D错误;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、化学键与能量关系为解答的关键,侧重分析与应用能力的考查,注意反应中断键与成键的判断,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
7.将足量CO2逐渐通入KOH和Ca(OH)2的混合溶液中,生成的物质依次是(水除外)( )
| A. | K2CO3、KHCO3、CaCO3、Ca(HCO3)2 | B. | CaCO3、K2CO3、KHCO3、Ca(HCO3)2 | ||
| C. | K2CO3、CaCO3、KHCO3、Ca(HCO3)2 | D. | K2CO3、CaCO3、KHCO3、Ca(HCO3)2 |
4.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X不同周期.下列说法一定正确的是( )
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | 物质W中Y化合价为+5价 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
11.下列有关药物的知识,说法正确的是( )
| A. | 麻黄碱是兴奋剂,奥委会严禁运动员使用 | |
| B. | 药物能防病治病,可以大量使用 | |
| C. | 胃酸分泌过多,可用氢氧化钠作抗酸药 | |
| D. | 使用青霉素前,不需进行皮肤敏感试验 |
1.下列关于16O与18O的叙述正确的是( )
| A. | 氧元素的相对原子质量为17 | |
| B. | 16O与18O核外电子排布方式不同 | |
| C. | 16O和18O的中子数分别为8和10 | |
| D. | 3.2 g16O2和3.2 g18O2均含有0.2NA个氧原子 |
8.丙烯醛(结构简式为CH2=CH-CHO)能发生的化学反应有( )
①加成 ②消除(消去) ③酯化 ④氧化 ⑤还原 ⑥加聚.
①加成 ②消除(消去) ③酯化 ④氧化 ⑤还原 ⑥加聚.
| A. | ②④⑤⑥ | B. | ③④⑤⑥ | C. | ①③⑤⑥ | D. | ①④⑤⑥ |
5.下列各组物质中,属于同系物的是( )
| A. | CH3OH、CH3OCH3 | B. | 醋酸、硬脂酸 | ||
| C. | CH3COOH、CH3CH=CHCO0H | D. | HCOOCH3、CH3COOH |
6. 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.
如图图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A. | 25℃时,相同浓度的CH3COONa溶液的碱性大于NaClO溶液 | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 导电能力:c>a | |
| D. | 图象中a点酸的总浓度小于b点酸的总浓度 |