题目内容
3.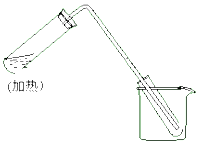 如图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中实验完全相同.回答下列问题:①左边试管中要加入几片碎瓷片,其作用是防止液体暴沸
②该装置中使用的玻璃导管较长,其作用是冷凝水蒸气;
③烧杯中还要盛有的物质是冰水混合物,作用是:使水蒸气充分冷凝.
分析 ①为防止液体暴沸,应加碎瓷片;
②玻璃导管除了起导气的作用,还起到了冷凝的作用;
③为了增强冷凝效果,可以用冰水混合物来充分冷凝水蒸气.
解答 解:①左边大试管中要加入几片碎瓷片,其作用是防止液体暴沸,
故答案为:防止液体暴沸;
②该装置中使用的玻璃导管较长,其作用是冷凝水蒸气,
故答案为:冷凝水蒸气;
③为了增强冷凝效果,烧杯中还要盛有的物质是冰水混合物,作用为使水蒸气充分冷凝,
故答案为:冰水混合物;使水蒸气充分冷凝.
点评 本题考查蒸馏水的制备,为高频考点,把握实验装置的作用、实验原理为解答的关键,侧重分析与实验能力的考查,注意仪器的作用及实验技能,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
12.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2 L的三氯甲烷所含的氢原子数为0.5NA | |
| B. | 7.2g丙烯酸分子中含有的双键数为0.2NA | |
| C. | 常温下,3.2g14C18O和16O2的混合物所含中子数为1.8NA | |
| D. | 足量Cu与Imol浓HNO3反应转移电子数目为0.5NA |
11.室温下,A、B两烧杯均盛有10mlpH=2的HA酸溶液,向B烧杯中加水稀释至pH=3,关于A、B两烧杯中溶液的描述正确的是( )
| A. | 水电离出的OH-浓度:10c(OH-)A>c(OH-)B | |
| B. | 溶液的体积:10VA≤VB | |
| C. | 若分别用等浓度的氢氧化钠溶液完全中和,所得溶液的pH:A>B | |
| D. | 若分别与10mLpH=12的氢氧化钠溶液反应,所得溶液的pH:A≤B |
18.下列溶液中有关物质的量浓度关系正确的是( )
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6 mol•L-1 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液,c(NaOH)<c(CH3COONa)<c(Na2CO3) | |
| C. | 0.2mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合:(H+)=c(OH-)+c(HCO3-)+2c(H2CO3) | |
| D. | 0.1 mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
12.下列物质在水溶液中的电离方程式中,正确的是( )
| A. | H2SO4=H2++SO42- | B. | Na2CO3=Na++CO32- | ||
| C. | NaHSO4=Na++H++SO42- | D. | Ca(OH)2=Ca2++2(OH)- |
 SiCl4在室温下为无色液体,易挥发,有强烈的刺激性气味.工业上,提纯粗硅的原理如下:粗硅$→_{△}^{HCl}$SiCl4$→_{△}^{Si+H_{2}}$SiHCl3$→_{△}^{H_{2}}$Si(纯)
SiCl4在室温下为无色液体,易挥发,有强烈的刺激性气味.工业上,提纯粗硅的原理如下:粗硅$→_{△}^{HCl}$SiCl4$→_{△}^{Si+H_{2}}$SiHCl3$→_{△}^{H_{2}}$Si(纯)