题目内容
将2.4g Fe、Mg 合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g.则收集到的气体体积V值不可能的是( )
| A、0.784 | B、0.896 |
| C、1.00 | D、1.12 |
考点:有关混合物反应的计算
专题:
分析:灼烧后得到的固体为Fe2O3和MgO的混合物,设出Fe、Mg的物质的量,然后根据质量计算出铁和镁的物质的量,再根据电子守恒讨论金属与硝酸反应生成NO的物质的量范围,当生成全部为亚铁离子时,得到的NO体积最少,当生成的全部为铁离子时,得到的NO体积最大,最后根据计算结果判断.
解答:
解:灼烧后得到的固体为Fe2O3和MgO的混合物,设Fe、Mg的物质的量分别为x、y,
则:56x+24y=2.4,
160×x×
+40y=3.6,
联立解得:x=0.03mol、y=0.03mol,
①当合金与稀硝酸反应生成的全部为亚铁离子时,金属失去的电子最少,则生成的NO体积最小,根据电子守恒,生成NO的物质的量为:
=0.04mol,标况下0.04molNO的体积为:22.4L/mol×0.04mol=0.895L;
②当合金与硝酸反应生成的全部为铁离子时,提供的电子的物质的量最大,则生成的NO的体积最大,根据电子守恒,生成NO的物质的量为:
=0.05mol,标况下0.05molNO的体积为1.12L,
所以生成的NO的体积范围为:0.896≤V(NO)≤1.12L,故不可能为0.784L,
故选A.
则:56x+24y=2.4,
160×x×
| 1 |
| 2 |
联立解得:x=0.03mol、y=0.03mol,
①当合金与稀硝酸反应生成的全部为亚铁离子时,金属失去的电子最少,则生成的NO体积最小,根据电子守恒,生成NO的物质的量为:
| 0.03mol×2+0.03mol×2 |
| 5-2 |
②当合金与硝酸反应生成的全部为铁离子时,提供的电子的物质的量最大,则生成的NO的体积最大,根据电子守恒,生成NO的物质的量为:
| 0.03mol×3+0.03mol×2 |
| 5-2 |
所以生成的NO的体积范围为:0.896≤V(NO)≤1.12L,故不可能为0.784L,
故选A.
点评:本题考查了有关范围讨论的计算,题目难度中等,明确铁与硝酸反应生成产物可能为亚铁离子或铁离子为解答关键,注意电子守恒在化学计算中的应用方法.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
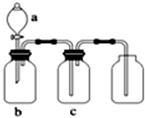 如图装置可用于制取、并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂)其中可行的是( )
如图装置可用于制取、并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂)其中可行的是( ) | 选项 | 气体 | a | b | c |
| A | 二氧化氮 | 浓硝酸 | 铜片 | 氢氧化钠溶液 |
| B | 二氧化硫 | 浓硫酸 | 铜片 | 酸性高锰酸钾溶液 |
| C | 氨 | 浓氨水 | 生石灰 | 碱石灰 |
| D | 二氧化碳 | 稀盐酸 | 碳酸钙 | 浓硫酸 |
| A、A | B、B | C、C | D、D |
下列实验操作中不正确的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,冷却水应从冷凝器下端进入 |
| C、蒸发时,要用玻璃棒不断搅动溶液 |
| D、过滤时,将待过滤的液体直接倒入漏斗,使液面低于滤纸的边缘 |
下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
| A、将pH=5的硫酸溶液稀释1000倍后,溶液中的SO42-与H+浓度的比值约为1:20 |
| B、0.1 mol/L NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2 c(CO32-) |
| C、将0.2 mol/L NaA溶液和0.1 mol/L盐酸溶液等体积混合所得溶液显碱性且有:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D、pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,由水电离出来的c(H+)相等 |
某植物含有机物X,其结构如图所示,下列说法中错误的是( )


| A、X分子中所有碳原子可能处在同一个平面上 |
| B、1 mol X与浓溴水反应时最多消耗2mol Br2 |
| C、X可以发生加成、加聚、氧化、还原、消去等反应 |
| D、1个X与足量H2完全反应的产物中含有3个手性碳原子 |
下列物质不能通过化合反应直接制得的是( )
| A、FeCl2 |
| B、NaHCO3 |
| C、H2SiO3 |
| D、Fe(OH)3 |
 低碳生活是一种时尚的生活理念,如何有效地开发利用碳资源以及降低大气中CO2的含量的研究显得更加紧迫.
低碳生活是一种时尚的生活理念,如何有效地开发利用碳资源以及降低大气中CO2的含量的研究显得更加紧迫.