题目内容
4. 某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( )
某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( )| A. | 一定有Fe2+,一定没有Fe3+、Mg2+ | |
| B. | 一定有Fe3+,一定没有Fe2+、Mg2+ | |
| C. | 一定有Fe3+,可能有Fe2+,一定没有Mg2+ | |
| D. | 一定有Fe2+,可能有Mg2+,一定没有Fe3+ |
分析 加入NaOH溶液,开始时有白色絮状沉淀生成,则不存在Fe3+,否则生成红褐色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色,说明含有Fe2+,由于红褐色可掩盖白色,则不能证明是否含有Mg2+,以此解答该题.
解答 解:加入NaOH溶液,开始时有白色絮状沉淀生成,则不存在Fe3+,否则生成红褐色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色,说明含有Fe2+,是亚铁离子的特征性质和反应现象,反应为:Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3,由于红褐色可掩盖白色,则不能证明是否含有Mg2+,
故选D.
点评 本题考查了常见离子的检验,为高频考点,题目难度中等,注意掌握常见离子的检验方法,熟记各种离子的特征反应,能够根据离子反应的特性正确推断离子种类.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
14.将4mol A气体和2mol B气体在2L的密闭容器中混合并在一定条件下发生反应:2A(g)+B(g)?2C(g),2s时测得C的浓度为0.6mol•L-1.下列说法正确的是( )
| A. | 用物质A表示的平均反应速率为0.3mol/(L•s) | |
| B. | 用物质B表示的平均反应速率为0.6mol/(L•s) | |
| C. | 2s时物质A的转化率为70% | |
| D. | 2s时物质B的浓度为0.7mol•L-1 |
15.A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.
(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
a的化学式为NaH;b的化学式为Na2O2和Na2C2;c的电子式为 ,d是金属晶体
,d是金属晶体
(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
(1)A在周期表位置第一周期第IA族,写出一种工业制备单质F的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为纯碱(或苏打),其水溶液与F单质反应的化学方程式为Cl2+2Na2CO3+H2O═NaClO+NaCl+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 ,d是金属晶体
,d是金属晶体(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为2mol.
12.钠与水反应的现象与钠的下列性质无关的是( )
| A. | 钠的熔点较低 | B. | 钠的密度小于水 | C. | 钠的硬度较小 | D. | 钠很活泼 |
19.下列物质中能够导电而且是电解质的是( )
| A. | 熔融的氢氧化钠 | B. | 稀盐酸 | C. | 硝酸钾晶体 | D. | 熔化的铁 |
9.下列说法正确的是( )
| A. | O2和O3互为同位素 | |
| B. | X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式为H3XO4 | |
| C. | HCl的形成过程用电子式表示为 | |
| D. | 铝与稀盐酸的反应既是氧化还原反应,又是放热反应 |
16.从海水提取溴的过程中,吸收塔内溴蒸气和吸收剂SO2发生的化学反应为:Br2+SO2+2H2O=2HBr+H2SO4,下列说法正确的是( )
| A. | SO2在反应中被还原 | B. | Br2在反应中失去电子 | ||
| C. | Br2在反应中表现氧化性 | D. | 1mol氧化剂在反应中得到1mol电子 |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1molFeCl2与1molCl2反应时转移的电子数为2NA | |
| B. | 2g H218O与D216O的混合物中所含电子数目为NA | |
| C. | 273K,101kPa下,28g乙烯与丙烯混合物中含有C-H键的数目为5NA | |
| D. | pH=1的H2SO3溶液10L,含H+的数目为2NA |
14.可用于鉴别以下三种化合物的试剂组合是( )
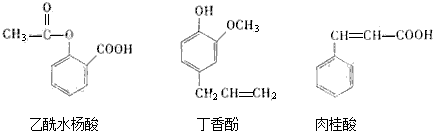
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④碳酸钠溶液.

①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④碳酸钠溶液.
| A. | ②与③ | B. | ③与④ | C. | ①与④ | D. | ②与④ |