题目内容
20.A、B、C、D、E是中学常见的物质.A由含淀粉的粮食发酵得到,C某种调味品的主要成分,它们之间的转化关系如图所示(反应条件及产物中的水已略去),请回答下列问题:(1)反应Ⅲ的有机反应类型是酯化反应或取代反应
(2)写出D→A+C的化学方程式:CH3COOCH2CH3+H2O$\stackrel{H+}{?}$CH3COOH+CH3CH2OH
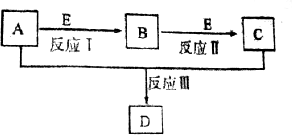
分析 A由含淀粉的粮食发酵得到为乙醇,C某种调味品的主要成分为乙酸,则E为O2,B为乙醛,D为乙酸乙酯,据此回答问题.
解答 解:A、B、C、D、E是中学常见的物质A由含淀粉的粮食发酵得到为乙醇,C某种调味品的主要成分为乙酸,则E为O2,B为乙醛,D为乙酸乙酯,反应Ⅰ、Ⅱ为氧化反应,反应Ⅲ为酯化反应或取代反应,
(1)分析可知反应为乙醇和乙酸发生的酯化反应或取代反应,故答案为:酯化反应或取代反应;
(2)D→A+C的反应为乙酸乙酯在稀酸溶液或碱溶液中水解,反应化学方程式:CH3COOCH2CH3+H2O$\stackrel{H+}{?}$CH3COOH+CH3CH2OH,故答案为:CH3COOCH2CH3+H2O$\stackrel{H+}{?}$CH3COOH+CH3CH2OH.
点评 本题考查了物质性质、物质转换关系,主要是有机物的氧化反应和酯化反应,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
10.下列关于电池的说法正确的是( )
| A. | 原电池负极金属一定比正极金属的金属性活泼 | |
| B. | 原电池中电解质溶液中的阳离子向负极移动 | |
| C. | 碱性锌猛锰干电池的负极反应为:Zn-2e-+4OH-=ZnO22-+2H2O | |
| D. | 铅蓄电池工作时转移电子数为2NA时,负极材料质量减少207g |
11.Wg10%的盐酸要使其浓度增大一倍,可采用的方法是( )
| A. | 再通入$\frac{W}{10}$g氯化氢 | B. | B、蒸发浓缩成$\frac{W}{2}$g | ||
| C. | 蒸发掉溶剂的一半 | D. | 再加入2Wg25%盐酸 |
8.X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数为20.下列判断正确的是( )
| W | X | Y |
| Z |
| A. | Z、X、Y形成的气态氢化物稳定性依次增强 | |
| B. | 四种元素形成的单质最多有6种 | |
| C. | 四种元素的原子半径:rZ>rY>rX>rW | |
| D. | 四种元素中,X的氧化物对应的水化物酸性最强 |
5.下列说法正确的是( )
| A. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增多 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使化学反应速率增大的主要原因是增加了反应物分子中活化分子的百分数 | |
| D. | 催化剂能增大单位体积内分子的总数,从而成千上万倍地增大反应速率 |
3.在氧化还原反应的过程中,氧化反应和还原反应同时发生,下列有关SO2-2e-+2H2O→SO42-+4H+的说法正确的是( )
| A. | 该反应为还原反应 | |
| B. | 上述反应中若产生0.1mol SO42-,则消耗SO2的物质的量为0.1mol | |
| C. | Fe2(SO4)3、品红两种溶液都能使上述反应进行 | |
| D. | 通入Cl2会增强SO2的漂白作用 |
 .
.