题目内容
13.在实验室进行教材中重点演示实验,括号内的实验仪器或试剂都能用到的是( )| A. | 验证牺牲阳极的阴极保护法(Fe电极、烧杯、K3[Fe(CN)6]溶液) | |
| B. | 铝热反应(漏斗、KClO3、铝粉) | |
| C. | 探究温度对化学平衡的影响(温度计、NO2球、烧杯) | |
| D. | 制氢氧化铁胶体(饱和FeCl3溶液、玻璃棒、胶头滴管) |
分析 A.牺牲阳极的阴极保护法,为原电池装置,Fe为负极,K3[Fe(CN)6]溶液可检验亚铁离子;
B.铝热反应中应点燃Mg条;
C.温度对化学平衡的影响,需要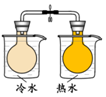 ;
;
D.制备胶体不能搅拌.
解答 解:A.牺牲阳极的阴极保护法,为原电池装置,Fe为负极,K3[Fe(CN)6]溶液可检验亚铁离子,实验仪器或试剂都能用到,故A正确;
B.铝热反应中应点燃Mg条,加入的氯酸钾为助燃剂,点燃镁时反应可发生,镁为引燃剂,Al片与金属氧化物反应,该铝热反应不能发生,故B错误;
C.温度对化学平衡的影响,需要冷水、热水,不需要温度计,故C错误;
D.制备胶体不能搅拌,不需要玻璃棒,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握原电池、平衡移动、胶体制备、铝热反应、实验技能为解本题关键,侧重分析与实验能力的考查,注意反应原理与实验的结合,题目难度不大.

练习册系列答案
相关题目
16.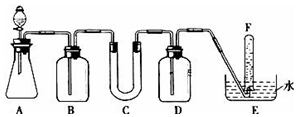 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
(1)填写表中空格:
已知A中放有碳酸钙,分液漏斗装稀盐酸
(2)为了达到实验目的,不需要(填“需要”或“不需要”)在B装置之后增加一个吸收水蒸气的装置;
(3)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂.
 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.(1)填写表中空格:
已知A中放有碳酸钙,分液漏斗装稀盐酸
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2气体中混入的HCl |
| C | 石棉绒与过氧化钠 | 与CO2反应,产生O2 |
| D | NaOH溶液 | 吸收未反应的CO2气体 |
(3)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂.
1.下列说法正确的是( )
| A. | 按系统命名法,化合物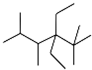 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 等物质的量的苯与苯甲酸完全燃烧消耗氧气的量不相等 | |
| C. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 | |
| D. | 已知C-C键可以绕键轴自由旋转,结构简式为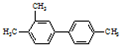 分子中有6个碳原子处于同一直线上 分子中有6个碳原子处于同一直线上 |
8.在下列实验操作中错误的是( )
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计的水银球靠近蒸馏烧瓶的瓶底 | |
| C. | 过滤时,玻璃棒在引流过程中应放在三层滤纸处 | |
| D. | 称量时,称量物置于托盘天平左盘,砝码放在托盘天平右盘 |
18.下列离子反应方程式中,属于水解反应的是( )
| A. | NH4++H2O=NH3•H2O+H+ | B. | CO32-+H2O?H2CO3-+2OH- | ||
| C. | HCO3-+H2O=H++CO32- | D. | CH3COO-+H2O?CH3COOH+OH- |
5.海带中含碘元素.从海带中提取碘有如下步骤:①通入适量Cl2;②将海带灼烧成灰后加蒸馏水搅拌;③加CCl4振荡;④过滤.合理的操作顺序是( )
| A. | ①②③④ | B. | ②①③④ | C. | ①③②④ | D. | ②④①③ |
2.在水溶液中能大量共存的一组离子是( )
| A. | Na+ Cl- NO3- H+ | B. | Na+ Cu2+ Cl- S2- | ||
| C. | K+ SO32- Fe3+ NO3- | D. | K+ Al3+ HCO3- SO42- |