题目内容
设阿伏加德罗常数的值为NA,则下列说法中正确的是( )
| A、加热条件下,1mol Cl2与足量Fe粉充分反应,转移的电子数为3NA |
| B、1 L浓度为1 mol?L-1的Na2CO3溶液中含有NA个CO32- |
| C、常温常压下,2.8g N2和2.8g CO所含电子数均为1.4NA |
| D、标准状况下,11.2L H2O中含有的原子数为1.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氯气和铁反应生成氯化铁,结合电子守恒计算分析;
B、碳酸根离子水溶液中水解;
C、氮气和一氧化碳没摩尔质量 相同为28g/mol,结合n=
计算物质的量,结合分子式计算电子数;
D、标准状况水不是气体;
B、碳酸根离子水溶液中水解;
C、氮气和一氧化碳没摩尔质量 相同为28g/mol,结合n=
| m |
| M |
D、标准状况水不是气体;
解答:
解:A、氯气和铁反应生成氯化铁,结合电子守恒计算,加热条件下,1mol Cl2与足量Fe粉充分反应,依据反应的氯气计算转移的电子数为2NA,故A错误;
B、碳酸根离子水溶液中水解,1 L浓度为1 mol?L-1的Na2CO3溶液中含有CO32-小于NA个,故B错误;
C、氮气和一氧化碳每摩尔质量相同为28g/mol,结合n=
计算物质的量=
=0.1mol,结合分子式计算,氮气中电子数0.1mol×2×7×NA=1.4NA,一氧化碳中电子数=0.1mol×(6+8)×NA=1.4NA,故C正确;
D、标准状况水不是气体,11.2L H2O物质的量不是0.5mol,故D错误;
故选C.
B、碳酸根离子水溶液中水解,1 L浓度为1 mol?L-1的Na2CO3溶液中含有CO32-小于NA个,故B错误;
C、氮气和一氧化碳每摩尔质量相同为28g/mol,结合n=
| m |
| M |
| 2.8g |
| 28g/mol |
D、标准状况水不是气体,11.2L H2O物质的量不是0.5mol,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的分析判断,气体摩尔体积条件应用,盐类水解分析,掌握基础是关键,题目较简单.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
R元素的一种粒子的结构示意图为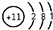 ,则下列说法不正确的是( )
,则下列说法不正确的是( )
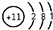 ,则下列说法不正确的是( )
,则下列说法不正确的是( )| A、该粒子容易得电子 |
| B、该粒子的核外有3个电子层 |
| C、R元素为金属元素 |
| D、R元素的原子有11个电子 |
在C(s)+CO2(g)═2CO(g)的反应中,现采取下列措施:①缩小容器体积;②增加碳的量;③通入CO2;④恒容下充入N2; ⑤恒压下充入N2,能够使反应速率增大的措施是( )
| A、①④ | B、②③⑤ |
| C、①③ | D、①②④ |
ClO2是一种广谱消毒剂,根据世界环保联盟的要求ClO2将取代Cl2成为生产自来水的消毒剂(Cl2能和水中溶解的某些有机物发生取代和加成反应,生成致癌物质).工业上常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得ClO2,以上反应中NaClO3和Na2SO3的物质的量比为 ( )
| A、1:1 | B、2:1 |
| C、1:2 | D、2:3 |
下列对酒精灯的使用方法的叙述错误的是( )
| A、加入酒精不超过容积的2/3 |
| B、可以用嘴吹灭火焰 |
| C、不用时须盖上灯帽 |
| D、禁止向燃着的酒精灯里添加酒精 |
小明因体内缺乏维生素A患了夜盲症,同学们纷纷地给他补充维生素A的食谱.下列食品对补充维生素A没有明显作用的是( )
| A、鱼肝油 | B、蛋黄 |
| C、绿叶蔬菜 | D、豆制品 |
标准状况下,在臭氧发生器中装入100mL O2,在一定条件下使之反应,最后又恢复到标准状况下,其体积为95mL,则最终混合气体的摩尔质量是( )
| A、32 g?mol-1 |
| B、33.7 g?mol-1 |
| C、48 g?mol-1 |
| D、40 g?mol-1 |
从保护人类的生存环境角度看,最好的燃料应是( )
| A、木材 | B、石油 | C、煤 | D、氢气 |



