题目内容
1 g氢气燃烧生成液态水,放出142.9 kJ热量,下列表示该反应的热化学方程式正确的是( )A.2H2(g)+O2(g)![]() 2H2O(l);ΔH=-142.9 kJ·mol-1
2H2O(l);ΔH=-142.9 kJ·mol-1
B.H2(g)+![]() O2(g)
O2(g)![]() H2O(l);ΔH=-285.8 kJ·mol-1
H2O(l);ΔH=-285.8 kJ·mol-1
C.2H2+O2![]() 2H2O;ΔH=-571.6 kJ·mol-1
2H2O;ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)![]() 2H2O(l);ΔH=+571.6 kJ·mol-1
2H2O(l);ΔH=+571.6 kJ·mol-1
B
解析:1 g氢气燃烧生成液态水放出142.9 kJ热量,则1 mol H2即2 g H2燃烧放出285.8 kJ热量,故有关热化学方程式为:H2(g)+![]() O2(g)
O2(g)![]() H2O(l);ΔH=-285.8 kJ·mol-1或2H2(g)+O2(g)
H2O(l);ΔH=-285.8 kJ·mol-1或2H2(g)+O2(g)![]() 2H2O(l);ΔH=-571.6 kJ·mol-1因此,A热量计算错误,B正确,C中状态未注明,D中ΔH表示错误。
2H2O(l);ΔH=-571.6 kJ·mol-1因此,A热量计算错误,B正确,C中状态未注明,D中ΔH表示错误。

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目


 (3)氢气热值为 。
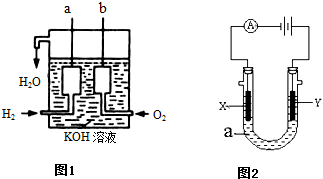
(3)氢气热值为 。  Ⅲ、右图表示一个电解池。X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液。
Ⅲ、右图表示一个电解池。X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液。