题目内容
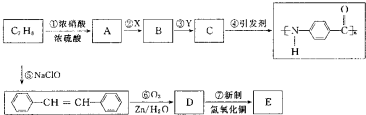
某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y.

已知: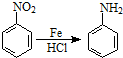 .2CH3CHO
.2CH3CHO
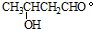
请回答下列问题:
(1)写出Y中含氧官能团的名称 .
(2)下列有关F的说法正确的是 .
A.分子式是C7H7NO2Br
B.既能与盐酸反应又能与NaOH溶液反应
C.能发生酯化反应
D.1mol F最多可以消耗2mol NaOH
(3)写出由甲苯→A反应的化学方程式 .
(4)在合成F的过程中,B→C步骤不能省略,理由是 ;
F在一定条件下形成的高分子化合物的结构简式是 .
(5)写出一种同时符合下列条件的Y的同分异构体的结构简式 .
①苯环上只有两种不同化学环境的氢原子②与足量浓溴水反应产生白色沉淀
③分子中只存在一个环状结构
(6)以X和乙烯为原料可合成Y,依次指出三步合成过程中三个主要反应的反应类型: 、 、 .

已知:
 .2CH3CHO
.2CH3CHO| NaOH |
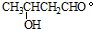
请回答下列问题:
(1)写出Y中含氧官能团的名称
(2)下列有关F的说法正确的是
A.分子式是C7H7NO2Br
B.既能与盐酸反应又能与NaOH溶液反应
C.能发生酯化反应
D.1mol F最多可以消耗2mol NaOH
(3)写出由甲苯→A反应的化学方程式
(4)在合成F的过程中,B→C步骤不能省略,理由是
F在一定条件下形成的高分子化合物的结构简式是
(5)写出一种同时符合下列条件的Y的同分异构体的结构简式
①苯环上只有两种不同化学环境的氢原子②与足量浓溴水反应产生白色沉淀
③分子中只存在一个环状结构
(6)以X和乙烯为原料可合成Y,依次指出三步合成过程中三个主要反应的反应类型:
考点:有机物的合成
专题:有机物的化学性质及推断
分析:由甲苯与B的分子式,结合D的结构简式可知,甲苯发生甲基对位的硝化反应生成A,则A为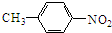 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化;甲苯与氯气在光照条件下发生的取代反应得到
,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化;甲苯与氯气在光照条件下发生的取代反应得到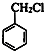 ,发生水解反应生成
,发生水解反应生成 ,再发生催化氧化生成
,再发生催化氧化生成 ,由信息可知,苯甲醛与乙醛在碱性条件下得到
,由信息可知,苯甲醛与乙醛在碱性条件下得到 ,再发生消去反应得到
,再发生消去反应得到 ,乙烯发生催化氧化生成乙醛,据此进行解答.
,乙烯发生催化氧化生成乙醛,据此进行解答.
 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化;甲苯与氯气在光照条件下发生的取代反应得到
,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化;甲苯与氯气在光照条件下发生的取代反应得到 ,发生水解反应生成
,发生水解反应生成 ,再发生催化氧化生成
,再发生催化氧化生成 ,由信息可知,苯甲醛与乙醛在碱性条件下得到
,由信息可知,苯甲醛与乙醛在碱性条件下得到 ,再发生消去反应得到
,再发生消去反应得到 ,乙烯发生催化氧化生成乙醛,据此进行解答.
,乙烯发生催化氧化生成乙醛,据此进行解答.解答:
解:由甲苯与B的分子式,结合D的结构简式可知,甲苯发生甲基对位的硝化反应生成A,则A为 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化,
,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化,
(1)由Y的结构可知,其含氧官能团的名称为醛基,故答案为:醛基;
(2)A.根据F的结构简式,可知其分子式应为C7H6NO2Br,故A错误;
B.F中有氨基与羧基,既能与盐酸反应又能与NaOH溶液反应,故B正确;
C.F中有羧基,能够发生酯化反应,故C正确;
D.羧基能与氢氧化钠反应,苯环上的溴原子很不活泼,难以与氢氧化钠反应,1molF能和1molNaOH反应,故D错误,
故答案为:BC;
(3)由甲苯→A反应的化学方程式为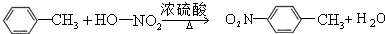 ,
,
故答案为: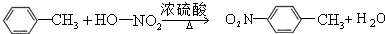 ;
;
(4)在合成F的过程中,氨基易被氧化,在氧化反应之前需先保护氨基,B→C步骤不能省略,F在一定条件下发生缩聚反应形成的高分子化合物,其结构简式为: ,
,
故答案为:氨基易被氧化,在氧化反应之前需先保护氨基; ;
;
(5)同时符合下列条件的Y( )的同分异构体与足量浓溴水反应产生白色沉淀,含有酚羟基,苯环上只有两种不同化学环境的氢原子,且分子中只存在一个环状结构,结合Y的结构简式可知,侧链中含有碳碳双键,含有2个不同的取代基且处于对,故符合条件的同分异构体为:
)的同分异构体与足量浓溴水反应产生白色沉淀,含有酚羟基,苯环上只有两种不同化学环境的氢原子,且分子中只存在一个环状结构,结合Y的结构简式可知,侧链中含有碳碳双键,含有2个不同的取代基且处于对,故符合条件的同分异构体为: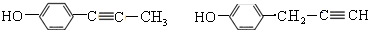 ,
,
故答案为: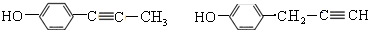 ;
;
(6)由信息可知,苯甲醛与乙醛在碱性条件下发生加成反应得到 ,再发生消去反应得到
,再发生消去反应得到 ,乙烯发生催化氧化得到乙醛,所以主要的反应类型为:氧化反应、加成反应、消去反应,
,乙烯发生催化氧化得到乙醛,所以主要的反应类型为:氧化反应、加成反应、消去反应,
故答案为:氧化反应;加成反应;消去反应.
 ,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为 ,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为 ,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为 ,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化,
,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化,(1)由Y的结构可知,其含氧官能团的名称为醛基,故答案为:醛基;
(2)A.根据F的结构简式,可知其分子式应为C7H6NO2Br,故A错误;
B.F中有氨基与羧基,既能与盐酸反应又能与NaOH溶液反应,故B正确;
C.F中有羧基,能够发生酯化反应,故C正确;
D.羧基能与氢氧化钠反应,苯环上的溴原子很不活泼,难以与氢氧化钠反应,1molF能和1molNaOH反应,故D错误,
故答案为:BC;
(3)由甲苯→A反应的化学方程式为
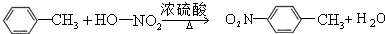 ,
,故答案为:
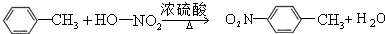 ;
;(4)在合成F的过程中,氨基易被氧化,在氧化反应之前需先保护氨基,B→C步骤不能省略,F在一定条件下发生缩聚反应形成的高分子化合物,其结构简式为:
 ,
,故答案为:氨基易被氧化,在氧化反应之前需先保护氨基;
 ;
;(5)同时符合下列条件的Y(
 )的同分异构体与足量浓溴水反应产生白色沉淀,含有酚羟基,苯环上只有两种不同化学环境的氢原子,且分子中只存在一个环状结构,结合Y的结构简式可知,侧链中含有碳碳双键,含有2个不同的取代基且处于对,故符合条件的同分异构体为:
)的同分异构体与足量浓溴水反应产生白色沉淀,含有酚羟基,苯环上只有两种不同化学环境的氢原子,且分子中只存在一个环状结构,结合Y的结构简式可知,侧链中含有碳碳双键,含有2个不同的取代基且处于对,故符合条件的同分异构体为: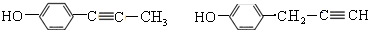 ,
,故答案为:
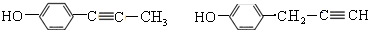 ;
;(6)由信息可知,苯甲醛与乙醛在碱性条件下发生加成反应得到
 ,再发生消去反应得到
,再发生消去反应得到 ,乙烯发生催化氧化得到乙醛,所以主要的反应类型为:氧化反应、加成反应、消去反应,
,乙烯发生催化氧化得到乙醛,所以主要的反应类型为:氧化反应、加成反应、消去反应,故答案为:氧化反应;加成反应;消去反应.
点评:本题考查有机合成,题目难度中等,充分利用有机物的分子式与结构分析解答,注意官能团的引入、消除与衍变,需要学生熟练掌握官能团的性质与转化.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
下列说法正确的是( )
| A、同一主族的金属元素,从上到下阳离子的氧化性逐渐增强 |
| B、最外层电子数相同的微粒,其化学性质一定相似 |
| C、同周期金属元素的氧化物对应水化物的碱性从左到右依次增强 |
| D、第ⅦA族元素从上到下,其氢化物稳定性减弱而还原性增强 |
“21金维他”中含有铁、钾、钙等多种成分,这里的铁、钾、钙是指( )
| A、单质 | B、元素 | C、分子 | D、原子 |
下列反应所得溶液中一定只含一种溶质的是( )
| A、向稀硝酸中加入铁粉 |
| B、向氯化铝溶液中加入过量的氨水 |
| C、向NaOH溶液中通入CO2气体 |
| D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液 |


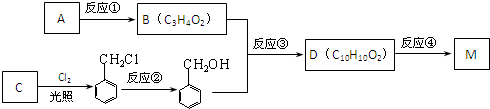
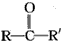 (R、R’代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如图1反应生成有机酸酯:
(R、R’代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如图1反应生成有机酸酯: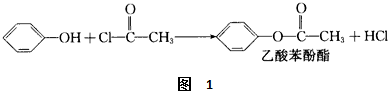
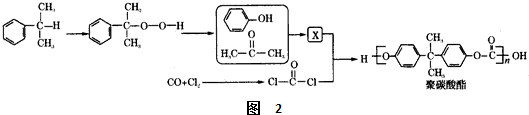
 反应合成聚碳酸酯的化学方程式
反应合成聚碳酸酯的化学方程式