题目内容
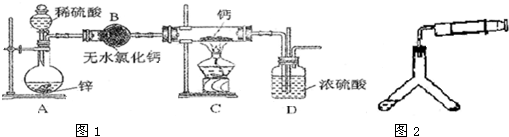
 下列关于如图所示装置的叙述,正确的是(水果电池示意图)( )
下列关于如图所示装置的叙述,正确的是(水果电池示意图)( )| A、铜是负极 |
| B、电能转变为化学能 |
| C、电子从铜片经导线流向锌片 |
| D、水果汁起到导电作用 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据原电池的工作原理来分析,原电池的工作原理:活泼金属为负极,失去电子,发生氧化反应,不活泼金属为正极,得到电子,发生还原反应;电子从负极沿导线流向正极,水果电池是将化学能转换成电能的装置.
解答:
解:A、活泼金属锌作负极,不活泼金属铜作正极,故A错误;
B、该装置为原电池,电池是将化学能转换成电能的装置,故B错误;
C、电子从负极沿导线流向正极,即电子从Zn流向Cu,故C错误;
D、该水果电池中果汁作电解质溶液,起到导电作用,故D正确;
故选D.
B、该装置为原电池,电池是将化学能转换成电能的装置,故B错误;
C、电子从负极沿导线流向正极,即电子从Zn流向Cu,故C错误;
D、该水果电池中果汁作电解质溶液,起到导电作用,故D正确;
故选D.
点评:本题考查了原电池工作原理,要会根据金属的活泼性来判断正负极,以及正负极上得失电子判断发生反应的反应类型、现象及电子流向等知识点,题目难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
下列各装置中,不能构成原电池的是( )
A、 盐酸 |
B、 硫酸铜溶液 |
C、 稀硫酸 |
D、 稀硫酸 |
在下列反应中,其离子方程式可以用H++OH-=H2O表示的是( )
| A、NaOH溶液与稀HNO3 |
| B、Cu(OH)2与稀HNO3 |
| C、NaOH溶液与CH3COOH溶液 |
| D、Ba(OH)2溶液与稀H2SO4 |
下列离子方程式书写正确的是( )
| A、少量的金属铜投入浓硝酸中Cu+4H++2NO3-=Cu2++NO2↑+2H2O |
| B、铝片投入稀盐酸中Al+6H+=Al3++3H2↑ |
| C、氢氧化钡溶液与稀硫酸混合Ba2++SO42-=BaSO4↓ |
| D、氢氧化铝与足量烧碱溶液混合Al(OH)3+OH-=AlO2-+2H2O |
下列物质的溶液中,pH最小的是( )
| A、乙酸 | B、乙酸钠 |
| C、氯化钠 | D、氢氧化钠 |
下列反应的离子方程式书写正确的是( )
| A、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| B、稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、碳酸钙与盐酸反应:2H++CO32-=H2O+CO2↑ |
| D、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
 ,比较它们的电子层数和核电荷数,按照Na、Mg、Al顺序排布,试解释它们金属性逐渐减弱的原因.
,比较它们的电子层数和核电荷数,按照Na、Mg、Al顺序排布,试解释它们金属性逐渐减弱的原因.