题目内容
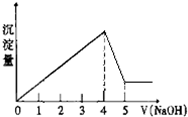 有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
考点:化学方程式的有关计算
专题:计算题
分析:氢氧化钠的体积为0~4时,发生的反应有:Al3++3OH-═Al(OH)3↓,Mg2++2OH-═Mg(OH)2↓,氢氧化钠的体积为4~5时发生的反应为:Al(OH)3+NaOH═NaAlO2+2H2O,假设氢氧化铝溶解消耗氢氧化钠为1mol,则沉淀最大时消耗NaOH为4mol,结合方程式计算n[Al(OH)3],进而计算n[Mg(OH)2],由原子守恒知n(Al)=n[Al(OH)3],n(Mg)=n[Mg(OH)2].
解答:
解:氢氧化钠的体积为0~4时,发生的反应有:Al3++3OH-═Al(OH)3↓,Mg2++2OH-═Mg(OH)2↓,氢氧化钠的体积为4~5时发生的反应为:Al(OH)3+NaOH═NaAlO2+2H2O,
假设氢氧化铝溶解消耗氢氧化钠为1mol,则沉淀最大时消耗NaOH为4mol,
由Al(OH)3+NaOH═NaAlO2+2H2O可知,n[Al(OH)3]=n(NaOH)=1mol,
Al3++3OH-═Al(OH)3↓
3mol 1mol
生成氢氧化镁沉淀消耗NaOH为4mol-3mol=1mol,由Mg2++2OH-═Mg(OH)2↓,可知n[Mg(OH)2]=0.5mol,
由原子守恒知n(Al)=n[Al(OH)3]=1mol,n(Mg)=n[Mg(OH)2]=0.5mol,
故原合金中镁、铝物质的量之比为0.5mol:1mol=1:2,
故选B.
假设氢氧化铝溶解消耗氢氧化钠为1mol,则沉淀最大时消耗NaOH为4mol,
由Al(OH)3+NaOH═NaAlO2+2H2O可知,n[Al(OH)3]=n(NaOH)=1mol,
Al3++3OH-═Al(OH)3↓
3mol 1mol
生成氢氧化镁沉淀消耗NaOH为4mol-3mol=1mol,由Mg2++2OH-═Mg(OH)2↓,可知n[Mg(OH)2]=0.5mol,
由原子守恒知n(Al)=n[Al(OH)3]=1mol,n(Mg)=n[Mg(OH)2]=0.5mol,
故原合金中镁、铝物质的量之比为0.5mol:1mol=1:2,
故选B.
点评:本题考查镁铝单质及其化合物的性质、混合物的有关计算,明确各阶段发生的反应是解题的关键,注意利用赋值法计算.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
下列关于物质“反应程度”的说法正确的是( )
| A、一定条件下,2mol SO2与足量O2反应可得到2mol SO3 |
| B、含4mol HCl的浓盐酸与足量的MnO2加热反应可制备1mol Cl2 |
| C、10mL 18.0mol/L H2SO4与足量铜加热反应可制备0.09mol SO2 |
| D、一定条件下,1mol N2与3mol H2反应可制备1.0mol NH3 |
“绿色化学”提倡化工生产应尽可能将反应物的原子全部利用,从根本上解决环境污染问题.在下列制备环氧乙烷的反应中,最符合“绿色化学”思想的是( )
A、CH2=CH2+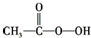 (过氧乙酸)→ (过氧乙酸)→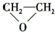 +CH3COOH +CH3COOH | ||
B、CH2=CH2+Cl2+Ca(OH)2→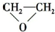 +CaCl2+H2O +CaCl2+H2O | ||
C、2CH2=CH2+O2
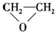 | ||
D、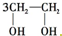
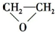 +HOCH2CH2-O-CH2CH2OH+2H2O +HOCH2CH2-O-CH2CH2OH+2H2O |
高氯酸是最强的酸,质量分数为60%的高氯酸溶液加热不分解,浓度增高就不稳定,受热易分解,热、浓的高氯酸溶液遇有机物易爆炸,纯高氯酸的沸点是130℃.现有市售的70%高氯酸,为使其进一步浓缩,所采取的措施正确的是( )
| A、加入浓硫酸后再小心常压蒸馏 |
| B、各仪器连接处的橡皮塞应塞紧防止漏气 |
| C、加入浓硫酸后再减压蒸馏 |
| D、加入浓硫酸后再加压蒸馏 |
已知NO+NO2+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO2+NaNO3+H2O.NO和NO2的混合气体的组成可表示为NOx,该混合气体通入NaOH溶液被完全吸收时,x的值为( )
| A、x≥1.5 | B、x=1.5 |
| C、x≤1.5 | D、无法确定 |