题目内容
3.在一密闭容器中,反应 a A(g)═b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,则下列判断不正确的是( )| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率减少了 | ||
| C. | 物质B的质量分数增加了 | D. | a<b+c |
分析 先假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的70%,比假设大,说明平衡向生成B的方向移动,即减小压强平衡向正反应方向移动,则a<b+c,据此结合选项判断.
解答 解:先假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的70%,比假设大,说明平衡向生成B的方向移动,即减小压强平衡向正反应方向移动,则a<b+c,
A、假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的70%,大于原来的50%,说明平衡向生成B的方向移动,即向正反应移动,故A正确;
B、根据A的判断,平衡向正反应移动,A的转化率增大,故B错误;
C、平衡向正反应移动,B的质量增大,混合气体的总质量不变,故物质B的质量分数增大,故C正确;
D、根据A的判断,平衡向生成B的方向移动,则a<b+c,故D正确;
故选B.
点评 本题考查化学平衡移动等,难度不大,注意利用假设法分析、判断平衡移动方向,掌握基础是解题关键.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
15.25℃时,下列溶液中水的电离程度最大的是( )
| A. | 0.01mol/L盐酸 | B. | pH=11氨水 | ||
| C. | pH=4NaHSO3溶液 | D. | 0.01mol/L Na2CO3溶液 |
13.在通常情况下不能共存,但均可用浓硫酸干燥的是( )
| A. | H2,H2S,SO2 | B. | N2,Cl2,HBr | C. | CO2,O2,NO | D. | NH3,CO2,HCl |
20.下列有机物中,含有两种官能团的是( )
| A. | CH2=CHCH2Cl | B. | CH3OH | C. | Cl-C2H4-Cl | D. | Br-CH=CH-Cl |
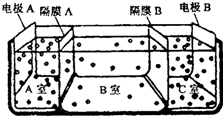
13. 某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )
某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )
 某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )
某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )| A. | 断开K1闭合K2时,总反应的离子方程式为:2H++2Cl-$\stackrel{电解}{→}$ H2↑+Cl2↑ | |
| B. | 断开K1闭合K2时,电子沿“a→Fe→电解质溶液→C→b”的路径流动 | |
| C. | 断开K1闭合K2时,铁电极附近溶液pH逐渐升高 | |
| D. | 断开K2闭合K1时,Fe电极被保护,此法称为牺牲阳极的阴极保护法 |
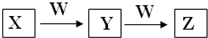 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系:
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系:
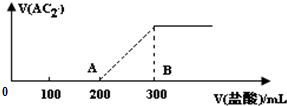 A、B、C、D、E为原子序数依次增大的五种短周期元素,A、B、C位于同一周期,C、E位于同一主族,A元素在自然界中形成的化合物种类最多,C元素的氢化物是最常用的溶剂,D元素在同周期元素中离子半径最小.请回答:
A、B、C、D、E为原子序数依次增大的五种短周期元素,A、B、C位于同一周期,C、E位于同一主族,A元素在自然界中形成的化合物种类最多,C元素的氢化物是最常用的溶剂,D元素在同周期元素中离子半径最小.请回答: ;D元素的最高价氧化物的水化物的电离方程式Al(OH)3?Al3++3OH-.
;D元素的最高价氧化物的水化物的电离方程式Al(OH)3?Al3++3OH-.