题目内容
12.现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下表:| 物质 | 熔点/℃ | 沸点/℃ | 密度/g/cm3 | 水中溶解性 |
| 甲 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | -84 | 87 | 0.90 | 可溶 |
| A. | 萃取法 | B. | 升华法 | C. | 蒸馏法 | D. | 分液法 |
分析 甲和乙沸点不同,且相差较大,可用蒸馏的方法分离,以此解答该题.
解答 解:由表中数据可知,甲和乙沸点不同,且相差较大,可用蒸馏的方法分离,而二者都溶于水,则不能用过滤、分液的方法分离.
故选C.
点评 本题考查物质的分离提纯,侧重于学生的分析、实验能力的考查,题目难度不大,注意把握表中数据,根据性质的异同选择分离方法.

练习册系列答案
相关题目
5.能正确表示下列反应的离子方程式是( )
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| B. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| D. | 明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓ |
4.下列叙述不正确的是( )
| A. | 在一瓣橘子上相隔0.5 cm分别插上一小块铜片和铝片,把铜片和铝片的另一端通过导线接触耳机的两极,能够从耳机中听到“嘎嘎”声 | |
| B. | 将两朵红色鲜花分别插入食用白醋和纯碱稀溶液中(每天更换上述稀溶液),几天后花的颜色有明显变化 | |
| C. | 将适量的食醋加入内壁有水垢的水瓶中,缓慢转动水瓶,一会儿水垢慢慢脱落 | |
| D. | 向25 mL沸水中滴加5~6滴稀的氯化铁溶液制备氢氧化铁胶体 |
20.传统的冰箱制冷剂“氟利昂”( CCl2F2)泄漏后台破坏臭氧层.其反应过程可表示为:03-→0+02;Cl+03→Cl0+02;ClO+O→Cl+02,总反应为203→302.则上述臭氧变成氧气的反应过程中,Cl原子的作用是( )
| A. | 氧化剂 | B. | 还原剂 | C. | 催化剂 | D. | 稳定剂 |
7.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成CH4燃料电池.已知通入CH4的一
极,其电极反应式是:CH4+10OH--8e-═CO32-+7H2O;下列叙述不正确的是( )
极,其电极反应式是:CH4+10OH--8e-═CO32-+7H2O;下列叙述不正确的是( )
| A. | 通入CH4的电极为负极 | |
| B. | 该电池使用一段时间后应补充KOH | |
| C. | 正极发生氧化反应 | |
| D. | 燃料电池工作时溶液中的阴离子向负极移动 |
17.下列物质长期露置在空气中,不会因为发生氧化还原反应而变质的是( )
| A. | Fe(OH)2 | B. | Na | C. | Na2O2 | D. | NaOH |
4.a、b、c、d是短周期元素,在周期表中的相对位置如图所示.c元素原子核外M层电子数是K层电子数的2倍.下列说法中,错误的是( )
| a | b |
| c | d |
| A. | 原子半径:c>b | |
| B. | 气态氢化物的稳定性:b>d | |
| C. | 高温下,a单质可与c的氧化物发生置换反应 | |
| D. | b的最高价氧化物对应的水化物中既含共价键又含离子键 |
1.如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )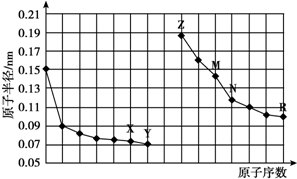

| A. | 简单离子的半径:X<Z<M | |
| B. | Y、R两种元素的气态氢化物稳定性:Y>R | |
| C. | 最高价氧化物对应水化物的酸性:R<N | |
| D. | 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
 b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,以下不正确的是( )
b B(g)+c C(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的70%,以下不正确的是( )