题目内容
2.査阅文献可知:白磷:分子式为P4,白色固体,着火点40℃,剧毒;红磷:巨型共价分子,棕红色 固体,着火点240℃,毐性较低;黑磷:空间网状结构,它将有可能替代传统的单晶硅成为电子线路的基本材料.它们的结构如下图所示: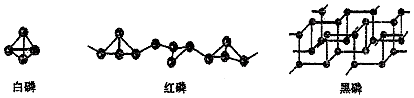
下列说法正确的是( )
| A. | 属于同位素 | B. | 属于同分异构体 | ||
| C. | 都属于多原子分子 | D. | 黑磷在空气中不易燃烧 |
分析 A.质子数相同中子数不同的同种元素的不同原子互称为同位素;
B.分子式相同,结构不同的有机物为同分异构体;
C.都是由原子构成的物质;
D.白磷着火点低易燃烧,红磷着火点高不易燃烧,黑磷结构分析可知为原子晶体,不易燃烧.
解答 解:A.白磷、红磷、黑磷为磷元素的不同单质,不是原子,不是同位素,故A错误;
B.结构分析可知分子式不同结构不同,不是同分异构体,故B错误;
C.都是多原子构成,但白磷为分子,红磷、黑磷不存在分子,故C错误;
D.黑磷结构分析可知为原子晶体,不易燃烧,故D正确;
故选D.
点评 本题考查了同位素、同素异形体、同分异构体,主要是结构的理解应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
12.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 2gH2中的原子数目为NA | |
| B. | 64gSO2中的原子数目为3NA | |
| C. | 1mol/LNaOH溶液中的Na+的数目为NA | |
| D. | 常温常下,11.2LCl2中的分子数目为0.5NA |
13.有机物甲、乙的结构如右图所示.下列说法错误的是( )
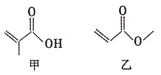
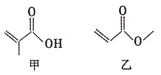
| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能发生取代、加成和水解反应 | |
| C. | 甲的一种同分异构体能发生银镜反应 | |
| D. | 等物质的量的甲和乙与足量的NaOH溶液反应,消耗NaOH的物质的量相等 |
10.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | n(H2CO3)和c(HCO3-)之和为1mol的NaHCO3溶液中,含有Na+数目为NA | |
| B. | 5g 21H和31H的混合物发生热核聚变反应:21H+31H→42He+10n,净产生的中子(10n)数为NA | |
| C. | 1L 0.1mol/L乙醇溶液中存在的共价键总数为0.8NA | |
| D. | 56g 铁与足量氯气反应,氯气共得到3NA个电子 |
17.已知甲苯的结构简式为 ,其二氯代物的同分异构体有( )
,其二氯代物的同分异构体有( )
 ,其二氯代物的同分异构体有( )
,其二氯代物的同分异构体有( )| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
7.下列实验操作、现象与所得结论一致的是( )
| 实验操作 | 现象 | 结论 | |
| A | 在试管中加入35mLNaAlO2溶液,再加入 过量稀盐酸,边加边振荡 | 溶液生成白色沉淀 | 制得A1(OH)3胶体 |
| B | 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液 | 前者溶液变蓝,后者有黄色沉淀 | KI3溶液中存在平衡:I3-?I2+I- |
| C | 将浓硫酸和乙醇混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 | 无明显现象 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
1.据科学家预测,月球的土壤中吸附着数百万吨的 3He,每百吨 3He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以 4He的形式存在.下列说法中正确的是( )
| A. | 4He原子核内含有4个质子 | |
| B. | 3He和4He互为同位素 | |
| C. | 3He原子核内含有3个中子 | |
| D. | 4He的最外层电子数为2,故4He具有较强的金属性 |
18.分子式为C6H12O且官能团为-CHO的有机化合物共有(不考虑立体异构)( )
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 9种 |