题目内容
15.下列有关强电解质叙述正确的是( )| A. | 强电解质在熔化状态下一定能够导电 | |
| B. | 离子化合物一定是强电解质 | |
| C. | 具有强极性键的共价化合物是强电解质 | |
| D. | 强电解质水溶液一定具有很强的导电能力 |
分析 A.强电解质是指水溶液中或熔融状态完全电离的电解质;
B.离子化合物是阴阳离子构成,水溶液中或熔融状态下一定能完全电离;
C.强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物,即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物,一般是强酸、强碱和大部分盐类;
D.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关.
解答 解:A.不含离子键的强电解质如HCl、AlCl3,在熔化状态下只存在分子一定不能够导电,故A错误;
B.离子化合物存在阴阳离子,水溶液中或熔融状态一定完全电离,属于强电解质,故B正确;
C.具有强极性键的共价化合物在水溶液中可能完全电离,如氯化氢属于强电解质,也可能部分电离,如HF是弱酸,水溶液中部分电离是弱电解质,故C错误;
D.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关,强电解质溶液的导电能力不一定比弱电解质溶液强如硫酸钡,难溶于水,其溶液离子浓度小导电能力弱,故D错误;
故选B.
点评 本题考查强电解质的性质判断,以及强电解质与溶液导电性的关系,题目难度不大,注意基础知识的积累,注意溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
5.NA代表阿伏伽德罗常数.已知C2H4和C3H6的混合物的质量为m g,则该混合物( )
| A. | 所含碳原子总数为$\frac{m{N}_{A}}{14}$ | |
| B. | 所含碳氢键数目为$\frac{3m{N}_{A}}{14}$ | |
| C. | 所含共用电子对数目为($\frac{m}{14}$+1)NA | |
| D. | 完全燃烧时消耗的O2一定是 $\frac{33.6m}{14}$L |
6.NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 标准状态下,33.6 L氟化氢中含有1.5 NA个氟化氢分子 | |
| B. | 1mol苯乙烯中含有的碳碳双键数为4NA | |
| C. | 1molNaCl晶体中含有NA个Na+ | |
| D. | 28g乙烯分子中含有极性共价键的数目为6NA |
3.下列各组离子能够大量共存且溶液呈无色的是( )
| A. | K+、Na+、Cl-、CO32- | B. | Mg2+、Al3+、OH-、SO42- | ||
| C. | H+、Ag+、Cl-、SO42- | D. | Fe2+、H+、Na+、NO3- |
10.下列图示的四种实验操作名称从左到右依次是( )
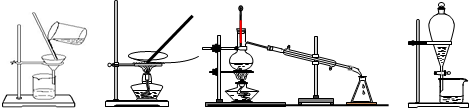

| A. | 过滤、蒸发、蒸馏、萃取分液 | B. | 过滤、蒸馏、蒸发、萃取分液 | ||
| C. | 蒸发、蒸馏、过滤、萃取分液 | D. | 萃取分液、蒸馏、蒸发、过滤 |
20.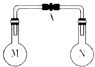 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )| 编号 | 1 | 2 | 3 | 4 |
| 气体M | H2S | NH3 | NO | H2 |
| 气体N | SO2 | HCl | O2 | Cl2 |
| A. | ①②③④ | B. | ②④①③ | C. | ④③①② | D. | ①④③② |
7.下列离子方程式正确的是( )
| A. | 硫化钠水解:S2-+2H2O?H2S+2OH- | |
| B. | 硫氢化钠的水解:HS-+H2O?H3O++S2- | |
| C. | 不断加热煮沸氯化铁溶液:Fe3++3H2O?Fe(OH)3+3H+ | |
| D. | NH4Cl水解:NH4++H2O?NH3•H2O+H+ |
5.下列括号中的物质是除去杂质所需的药品,其中错误的是( )
| A. | NaCl溶液中有杂质Na2SO4(氯化钡) | B. | FeS04溶液中有杂质CuSO4(铁粉) | ||
| C. | 生石灰中混有少量石灰石(盐酸) | D. | BaCl2溶液中有少量MgCl2(氢氧化钡) |